| المجلد 3 , العدد 9 , رمضان 1426 - تشرين الأول (أكتوبر) 2005 |
| |
| البيغفيلغراستيم: التطورات الأخيرة في المعالجة الاتقائية لقلة العدلات المُحَرّض بالمعالجة الكيميائية |
| Pegfilgrastim: Recent Advances in the Prophylaxis of Chemotherapy-Induced Neutropenia |
| ترجمة د. عماد أبو عسلي |
| Abou-Asaleh I. |
كلية الطب – جامعة دمشق
عن مقال من مجلة Supportive Cancer Therapy, 2 (3): 149-152, 2005 |
| الملخص Abstract |
يعد كبت النقي Myelosuppression المُحَّرض بالمعالجة الكيميائية السَّامة للخلايا التأثير الجانبي الأكثر شيوعاً الذي يتعلق بالجرعة عند معالجة السرطان وهو غالباً ما يكون مترافقاً مع قلة العدلات Neutropenia والعداوى. ويمكن لحدوث قلة العدلات الحُمّوي (F.N) Febrile Neutropenia أن يؤدي إلى تخفيض الجرعة وإلى تأخير دورات المعالجة الكيميائية المساعدة اللاحقة، الأمر الذي قد يكون له تأثير غير مرغوب به فيما يتعلق بديمومة الحياة عموماً وفي عدم الحاجة للدواء خلالها. ومن أجل المساعدة في منع حدوث قلة العدلات يمكن أن يُعالج المرضى الذين لديهم معدل اختطار مرتفع للإصابة بالعداوى الناجمة عن المعالجة الكيميائية بعوامل النمو الاتقائية المكوِّنة للدم مثل العامل المنبه لمستعمرات الخلايا المحببة granulocyte colony-stimulating factor (G-CSF) والعوامل المكوِّنة للحمر.
الفيلغراسيتم filgrastim هو العامل G-CSF البشري المأشوب الذي استعمل بشكل واسع في تدبير قلة العدلات المُحَرَّض بالمعالجة الكيميائية، ومع ذلك فإن عمره النصفي القصير (3.5 ساعات) يجعل من الضروري إعطاءه يومياً بجرعة تحت الجلد أو ضمن الوريد وحتى يتم استرداد العدلات، مما يتسبب بحدوث مصاعب إضافية للمرضى الذين هم مرهقين مسبقاً من المعالجة الكيميائية الكابتة للنقي. ولجعل الفعالية بالمستوى الأمثل وللتغلب على المصاعب المترافقة مع إعطاء الفيلغراستيم، تم تطوير شكلاً من البيغفيلغراستيم (P.F) ذي التأثير المديد من خلال تكنولوجيا إيلاج الاسفين pegylation technology، التي يتم فيها تعديل الفيلغراستيم بمزاوجته بجزيئات عديد الإيثيلين غليكول (3).
لقد أظهرت العديد من التجارب السريرية أن P.F المعطى كجرعة واحدة في دورة المعالجة الكيميائية، كجرعة ثابتة أو اعتماداً على الوزن، كان فعالاً كإعطاء الجرعة اليومية من الفيلغراستيم عند تدبير قلة العدلات المحرض بالمعالجة الكيميائية. وقد أبدى مرضى سرطان الثدي المتلقين للمعالجة الكيميائية بجرعة وحيدة من P.F تعداداً مماثلاً لذلك التعداد الملاحظ عند المرضى المتلقين للفيلغراستيم يومياً (5). بالإضافة إلى ذلك، فقط لوحظ وجود معدل منخفض بشكل يُعتد به من حدوث F.N عند المعالجة بالـ P.F مقارنة مع الفيلغراستيم (9% مقابل 18%، P= 0.029) (6)، كما شوهد أيضاً شكلاً مقبولاً من السمّية عند المعالجة بالـ P.F على نحو مماثل لذلك الذي للفيلغراستيم.
تقوم التجارب السريرية حالياً بتوسيع الخبرة السريرية للمعالجة بالـ P.F في ضروبٍ من الأورام الصلبة وأمراض الدم الخبيثة. فقد جرى في الندوة السنوية السابعة والعشرين حول سرطان الثدي في مدينة سان انطونيو، عرض العديد من التجارب التي أعطت أفكاراً جديدة عن برامج إعطاء الدواء والفائدة السريرية للـ P.F عند مرضى سرطان الثدي المتلقين المعالجة الكيميائية الكابتة للنقي وقد قمنا هنا بإيجاز هذه التجارب.
اعطاء P.F في اليوم ذاته مقابل إعطاؤه في اليوم التالي إلى جانب الدوسيتاكسيل / الدوكسوروبيسين/ السيكلوفسفاميد في المرحلة المبكرة والمتقدمة لسرطان الثدي.
توفر المعالجة الكيميائية بالـ TAC (اختصاراً لدوسيتاكسيل / دوكسوروبيسين / سيكلوفسفاميد) بُقيا إجمالية لحياة مرضى سرطان الثدي من المرحلة الباكرة ومع هذا فإن TAC يترافق مع نسبة مرتفعة لحدوث F.N، مما يستوجب إجراء تعديلات علاجية والإدخال للمستشفى والمعالجة بالمضادات الحيوية. إلا أن المرضى المتلقين لـ TAC يُعالجون روتينياً بالـ P.F الاتقائي في اليوم الثاني من إعطاء المعالجة الكيميائية بسبب ظهور حالة F.N في هذا النمط العلاجي. وهنا يبرز السؤال التالي: هل من المحتمل أن يكون إعطاء P.F في ذات يوم إعطاء المعالجة الكيميائية آمناً وفعالاً في تدبير قلة العدلات المحرَّضة بالمعالجة الكيميائية؟
في هذا الإطار قام كوفمان Kaufman وزملاؤه بتجربة من الطور الثاني العشوائي – بتقييم الفائدة السريرية لإعطاء العلاج باليوم ذاته مقابل إعطاء كل من الـ P.F مع الـ TAC في اليوم التالي عند نساء مصابات بسرطان الثدي في المرحلة الباكرة أو المتقدمة (7). وقد جرى توزيع مرضى سرطان الثدي بالمراحل II-IV واللاتي كنَّ مرشحات للعلاج بـ TAC (دوسيتاكسيل 75 ملغ / م2، دوكسوروبيسين 50 ملغ / م2، سيكلوفسفاميد 500 ملغ / م2)، تمَّ توزيعهن عشوائياً لتلقي P.F (6 ملغ) خلال 4 ساعات أو 24 ساعة تقريباً بعد إعطاء المعالجة الكيميائية، وذلك في دراسة عالية السريّة. وقد كانت النقطة النهائية الأولية هي فترة دوام حالة قلة العدلات من الدرجة الرابعة في الدورة الأولى من المعالجة الكيميائية. بالإضافة إلى ذلك فقد تم تضمين كل من فترة دوام قلة العدلات في الدورة الثالثة وحدوث F.N وحصول حوادث غير مرغوب فيها كنقاط نهائية ثانوية في هذه الدراسة التي جرى فيها توزيع العدد الإجمالي للمرضى البالغ 93. وقد بينت الدراسة أنه بالمقارنة مع إعطاء P.F في اليوم التالي، فإن إعطاؤه في اليوم ذاته كان أقل فاعلية في تخفيض فترة دوام قلة العدلات الوخيم، كما كان ذلك مترافقاً مع
حدوث نسب مرتفعة لـ F.N. وقد كانت فترة دوام قلة العدلات من الدرجة الرابعة في الدورة العلاجية الأولى 2.4 يوماً عند المرضى المتلقين للـ P.F في اليوم ذاته و 1.4 يوماً عند المرضى المتلقين له في اليوم التالي (الجدول 1).
وقد لوحظ وجود اختلافات مماثلة في فترة دوام قلة العدلات (الدرجة الرابعة) بين إعطاء P.F في اليوم ذاته مقابل إعطاؤه في اليوم التالي في المعالجة الكيميائية (الدورة الثالثة).
لقد سجل حدوث F.N عند المرضى المتلقين للـ P.F في اليوم ذاته بنسبة 22% مقارنة مع 7% عند المرضى المتلقين له في اليوم التالي خلال الدورة الأولى من المعالجة الكيميائية (الجدول 1). وكانت نسبة حدوث F.N في الدورة الثالثة من المعالجة الكيميائية أقل بشكل معتد به، لكن كانت هذه
|
الجدول 1: الاتقاء بالـ P.F في اليوم ذاته مقابل اليوم التالي: حدوث قلة العدلات عند مرضى سرطان الثدي (7).
الحدث |
اليوم ذاته |
اليوم التالي |
فترة دوام قلة العدلات (الدرجة الرابعة) |
2.4 يوماً |
1.4 يوماً |
قلة العدلات الحموي الدورة 1 |
10 (22%) |
3 (7%) |
الدورة 3 |
3 (8%) |
1 (2%) |
كل الدورات |
15 (33%) |
5 (11%) |
F.N المتعلقة بالدخول للمستشفى / باستخدام المضادات الحيوية وريدياً (كل الدورات) |
10 (22%) |
3 (7%) |
|
النسبة عند المرضى المتلقين للـ P.F أعلى في اليوم ذاته مما لدى المتلقين له في اليوم التالي (8% مقابل 2%). وبشكل عام فإن نسبة حدوث F.N بكل دورات المعالجة الكيميائية كانت أعلى بشكل ملحوظ عند المرضى المتلقين للـ P.F في اليوم ذاته مما عند المتلقين له في اليوم التالي (33% مقابل 11%). إضافة إلى ذلك فإن F.N التي تطلبت الإدخال للمستشفى أو لتلقي المضادات الحيوية وريدياً كانت أكثر شيوعاً عند المرضى المتلقين للـ P.F في اليوم ذاته مقارنة مع المرضى المتلقين له في اليوم التالي (22% مقابل 7%)، ولم يُلاحظ حدوث قلة الصفيحات الدموية المتزايد، فيما عدا أن إعطاء العلاج في اليوم ذاته هو أمر فعال ومأمون بشكل مؤكد في التقارير البحثية الأخرى، فإن الدراسة الحالية تؤكد على الممارسة المنصوح بها لإعطاء P.F في اليوم التالي للمعالجة الكيميائية الكابتة للنقي بشكل كبير. بالإضافة إلى أن تجارب الطور II العشوائية تتقدم باستمرار مقارنة بـ P.F اليوم التالي مع خطط المعالجة الكيميائية الأخرى.
استخدام البيغفيلغراستيم P.F في الدورة الأولى والدورات التالية يمنع حدوث F.N عند مرضى سرطان الثدي المعانين من المعالجة الكيميائية الكابت للنخامية.
قام فوغل Vogel وزملاؤه بإجراء دراسـة
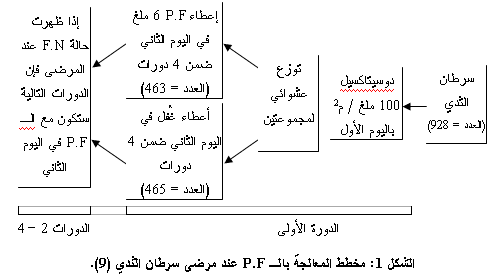
عشوائية من الطور الثالث لتقييم استخدام P.F جنباً إلى جنب وبدءاَ من الدورة الأولى والدورات التالية مع المعالجة الكيميائية الكابتة للنخامية من أجل إنقاص وقوع قلة F.N عند مرضى سرطان الثدي. وقد نُشرت نتائج هذه الدراسة مؤخراً (8) وعُرضت في مؤتمر سرطان الثدي السنوي السابع والعشرين سان انطونيو (9)، حيث تم توزيع المرضى المختارين عشوائياً لتلقي جرعة من P.F (6 ملغ) تحت الجلد أو لتلقي علاجاً ارضائياً مرة واحدة في الدورة العلاجية وذلك في اليوم الثاني بعد إعطاء 100 ملغ / م2 من الدوسيتاكسيل (اليوم 1: الشكل 1) (9). وقد تلقى المرضى 4 دورات كحد أعلى ممن البروسيتاكسيل كل 3 أسابيع.
كان عدد المرضى الإجمالي 928 بمتوسط عمر 52 عاماً وعدد المتلقين للـ P.F (العدد = 463) أو الغفل placebo (العدد 465)، وكان التوازن جيداً بين هاتين المجموعتين، حيث كانت النسبة التقريبية للمعانين من الداء النقيلي 60% في كلتي المجموعتين، وقد تلقى ثلثي المرضى في المجموعتين علاجاً كيميائياً.
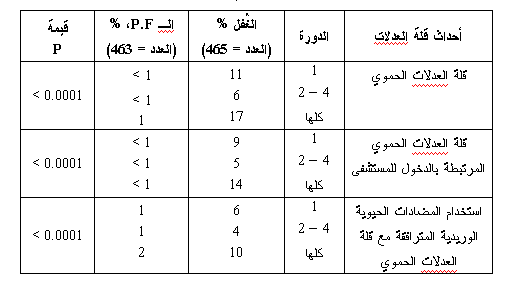
أدى استخدام الـ P.F إلى تخفيض واضح في نسبة حدوث F.N عند مرضى سرطان الثدي (الجدول 2) (9)، وكانت نسبة F.N 1% عند المرضى المتلقين للـ P.F مقابل 17% عند المتلقين للغفل (0.0001 > P). وقد تراجعت أعداد المرضى الملتحقين بالمستشفيات بسبب F.N وانخفض استعمال العوامل الوريدية المضادة للأخماج بشكل واضح في المجموعة المتلقية للـ P.F (1% و 2% على الترتيب) مقارنة مع المجموعة المتلقية للغفل (14% و 10% على الترتيب، 0.0001 > p).
وبشكل عام فإن F.N قد ظهرت في الدورة الأولى، التي فيها 11% من مرضى مجموعة الغفل عانوا من F.N مقرنة مع %1> عند المجموعة المتلقية للـ P.F. أما في الدورات 2 – 4 فإن نسبة حدوث F.N بلغت 6% (في الغُفل) مقابل %1> في مجموعة الـ P.F. بالإضافة إلى ذلك، فإن نسبة حدوث قلة العدلات من الدرجة 4 / 3 قد انخفضت بشكل ملموس عند المرضى المتلقين للـ P.F خلال كل الدورات. لذلك فإن الدراسة التي بينت أن استخدام P.F في الدورة الأولى والدورة التالية إلى جانب خطة المعالجة الكيميائية الكابتة للنقي بشكل معتدل للمادة النخامية قد أدى إلى تخفيض مُعتد به في نسبة حدوث F.N وإلى تقليل أعداد المرضى المسجلين في المستشفيات بسبب F.N، وإلى تقليل استخدام العوامل الوريدية المضادة للعداوى عند مرضى سرطان الثدي.
استخدام عوامل النمو طويلة التأثير والـ P.F والداربيبويتين ألفا Darbepoetin في المعالجة الكيميائية المساعدة كثيفة الجرعات
لمعالجة الكيميائية كثيفة الجرعات فائدة واضحة في العلاج المساعد لسرطان الثدي. وتُُعد المعالجة الكيميائية المسـاعدة كثيـفة
الجرعات أمراً ضرورياً لتستطيع عوامل النمو تأمين استرداد العدلات (تعداداً). كما تؤدي المعالجة الكيميائية متكررة الجرعات أيضاً إلى تخفيض فترة استرداد الكريات الحمرا، مما يقود إلى الاستخدام المتكرر لعوامل النمو الحمرائية. وهذه السمّية الدموية بالإضافة إلى الانزعاج من الجرعات اليومية للفيلغراسيتم ولعدة أسابيع يجعل من أداء المعالجة الكيميائية كثيفة الجرعات أمراً أكثر تعقيداً بعض الشيء من العلاج المعياري لفترة ثلاثة أسابيع. وقد بينت تجربة الطور الثاني أهمية استخدام الـ P.F والداربيبويتين ألفا، يُعطى كل منهما كل أسبوعين، في تأمين المعالجة الكيميائية لمرضى سرطان الثدي من المرحلة I-III لكل أسبوعين (10).
عولج مرضى سرطان الثدي بالمعالجة الكيميائية كثيفة الجرعات مع الدوكسوروبيسين (60 ملغ / م2) والسيكلوفسفاميد (600 ملغ / م2) المتبوعين بالباكليتاكسيل paclitaxel (175 ملغ / م2) كل أسبوعين لأربع دورات، وهذا النظام مماثل لذلك المستخدم في التجربة 9741 لسرطان ابيضاض دم المجموعة B (GALG B) (11). وقد تلقى المرضى الـ P.F (6 ملغ) تحت الجلد في اليوم الثاني من كل دورة علاجية وبُدأ لهم بالداربيبويتين ألفا بجرعة أولية 200 مكغ من أجل مستويات هيموغلوبين الدم 12 غ / دل، ثم بحسـب
الخطة الحسابية الموضوعة (الشكل 2) (10).
لقد استوفى اختبار الطور II هدفه عند 135 مريضاً وكل المرضى المنهين للنظام العلاجي الموضوع. وكانت نسبة حدوث F.N < 2% (حالتان إجمالاً) وهي متوافقة مع نتائج التجارب المجراة سابقاً على إعطاء الفليفراستيم ذو الـأثير فصير ألأمد والمعطى في الأيام 3 – 10 في كل دورة إلى جانب المعالجة الكيميائية الموضوعة ذاتها. وقد أدى الإعطاء المبرمج للداربيبويتين ألفا إلى التماشي التام لحدوث حالات نقل كريات الدم الحمر عند المرضى المعالجين، وكانت نسبة المرضى الذين تلقوا (D.A) أولاً < 90%، وكانت المستويات الوسيطية للهيموغلوبين ضمن مجال 11 – 12 غ / دل بشكل دائم. وقد أظهرت عوامل النمو المكونة للدم طويلة التأثير والـ P.F والـ D.A فاعلية وأماناً في تسهيل المعالجة الكيميائية المساعدة كثيفة الجرعات مع الدوكسوروبيسين والسيكلوفسفاميد المتبوعين بالباكليتاكسيل.
|
 |
الأهمية السريرية للموضوع.
أظهر هذا الاختبار أن عوامل النمو طويلة التأثير ولـ P.F و الـ D.A يمكن أن تكون فعالة وأمينة عند إعطائها لمرضى سرطان الثدي المتلقين للمعالجة الكيميائية كل أسبوعين بكل من الدوكسوروبيسين / السيكلوفسفاميد المتبوع بالباكليتاكسيل. وكان الـ P.F الوقائي فعال بشكل كبير في تخفيض F.N، مع حصول سمية مقبولة عندما يُستخدم بالدورة الأولى والدورات التالية من المعالجة الكيميائية بالدوسيتاكسيل عند مرضى سرطان الثدي. ومع ذلك فإن إعطاء الـ P.F في اليوم ذاته كان مترافقاً مع خسارة الفائدة السريرية بالمقارنة مع إعطائه في اليوم التالي من أجل تخفيض فترة بقاء قلة العدلات الوخيم ونسبة حدوث قـلة العدلات الحموي عند مـرضى سرطان الثدي المتلقين للعلاج الكيميائي بالـ TAC. وكان المعالجة الاتقائية بالـ P.F المُعطى بعد يومٍ من إعطاء المعالجة الكيميائية
|
الجدول 2: الاتقاء بالـ P.F: نسبة حدوث قلة العدلات عند مرضى سرطان الثدي (9).

الشكل 2: كيفية حساب الـ Darbepoetin (D.A): تقييم الهيموغلوبين كل أسبوعين (10). |
* المرضى الذين أُوقف لهم D.A من أجل مستويات خضاب الدم > 12 غ / دل والذين سيبدأون من جديد بالـ D.A في الأسابيع اللاحقة، سوف يبدأون به من جديد بنسبة 75% من الجرعة الأخيرة.
أكثر فاعلية وأظهرت حالة مريحة تماماً أكثر من الإعطاء اليومي للفيلغراستيم قصير أمد التأثير عند المرضى المتلقين لبرامج المعالجة الكيميائية الكابتة للمادة النخامية والمترافقة مع ? 20% من اختطار حدوث F.N.
|
| المراجع Reference |
1-Crawford J.
Once-per-cycle pegfilgrastim (Neulasta) for the management of chemotherapy-induced neutropenia.
Semin Oncol, 30(4 suppl 13): 24-30, 2003.
2-Patton J; Reeves T. and Wallace J.
Effectiveness of darbepoetin alfa versus epoetin alfa in patients with chemotherapy-induced anemia treated in clinical practice.
Oncologist, 9: 451-458, 2004.
3-Molineux G; Kinstler O. and Briddell B.
A new form of filgrastim with sustained duration in vivo and enhanced ability to mobilize PBPC in both mice and humans.
Exp Hematol, 27: 1724-1734, 1999.
4-Biganzoli L; Untch M. and Skacel T.
Neulasts (pegfilgrastim): a once-per-cycle option for the management of chemotherapy-induced neutropenia.
Sernin Oncel, 31(3 suppl 8): 27-34, 2004.
5-Green MD; Koelbl H. and Baselga J.
A randomized double-blind multicenter phase III study of fixed-dose single-administration pegfilgrastim versus daily filgrastim in patients receiving myelosuppressive chemotherapy.
Ann Oncol, 14: 29-35, 2003.
6-Holmes PA; O’Shaughnessy JA. and Vukelja S.
Blinded, randomized, multicenter study to evaluate single administration pegfilgrastim once per cycle versus daily filgrastim as an adjunct to chemotherapy in patients with high-risk stage II or stage III/IV breast cancer.
J Clin Oncol, 20: 727-731, 2002.
7-Kaufman PA; Paroly W. and Rinaldi D.
Randomized double-blind phase 2 study evaloaring same-day vs. next-day administration of pegfilgrastim with docetaxel, doxorubicin, and cyclophosphamide (TAC) in women with early stage and advanced breast cancer.
Breast Cancer Res Treat 2004; 88 (suppl 1): S59 (Abstract #1054).
8-Vogel CL; Wojtukiewicz MZ. And Carroll RR.
First and subsequent cycle use of pegfilgrastim prevents febrile neutropenia in patients wieh breast cancer: a mulricenter,
double-blind, placebo-controlled phase Ill study.
Clin Oncsl, 23: 1178-1184, 2005.
9-Vogel C; Rader M. and Tyulandin S.
Pegfilgrastim nearly abrogates occurrence of neutropenic events early in the course of chemotherapy: results of a phase 3, randomized, double-blind, placebo-controlled study of patients with breast cancer receiving docetaxel.
Breast Cancer Ret Treat 2004; 88 (suppl 1):S1 (Abstract #5044).
10-Burstein HJ; Parker LM. and Doherty J.
Use of the long-acting hematopoietic growth factors pegfilgrastim and darbepoetin atfa in support of dose-dense adjuvanr chemotherapy.
Breast Cancer Res Treat 2004; 88 (suppl 1): S60 (Abstract #1055).
11-Citron ML; Berry DA. and Cirrincione C.
Randomized trial of dose-dense versus conventionally schduled and sequential versus coencurrent combination chemotherapy as postoperative adjuvant treatment of node-positive primary breast cancer: first report of Intergroup Trial C974 1/Cancer and Leukemia Group B Trial 9741.
J Clin Oncl, 21: 1431-1439, 2003.
|
| |
| المجلد 3 , العدد 9 , رمضان 1426 - تشرين الأول (أكتوبر) 2005 |
|
|
|
