| المجلد 4 ,
العدد 3
, رمضان 1427 - تشرين الأول (أكتوبر) 2006 |
| |
دراسة العلاقة بين مستوى الهيموغلوبين الغلوكوزي (HbA1c)
والإجهاد التأكسدي في الداء السكري نمط II
|
Studying the Relationship between HbA1c Level
and Oxidative Stress in Type II Diabetes Mellitus
|
| د. عدنان حموي |
| Hamwi Adnan |
| كلية الطب – جامعة دمشق |
| الملخص Abstract |
| درسنا العلاقة بين مستويات HbA1c ودرجة الإجهاد التأكسدي عند مرضى الداء السكري النمط II، وأظهرت هذه الدراسة وجود علاقة ارتباط خطية طردية بين مستوى شحميات المصل المرتفعة والإجهاد التأكسدي (مستوى TBARS)؛ ووجود علاقة خطية طردية بين TBARS ومستويات الهيموغلوبين الغلوكوزي؛ وعلاقة عكسية بين TAS و HbA1c. نقترح أن زيادة مستوى الاجهاد التأكسدي عند السكريين عموماً وبخاصة عند مفرطي شحميات الدم منهم يؤدي إلى ارتفاع مستوى HbA1c بشكل جزئي وبغض النظر عن مستويات غلوكوز الدم. تشير مستويات TAS إلى أهمية الفيتامينات المضادة للتأكسد بخاصة E و C في انقاص مستوى الاجهاد التأكسدي وبالتالي في انقاص مستويات HbA1c عند السكريين. |
| We have studied the relationship between HbA1c levels and oxidative stress degree in Type II diabetes mellitus patients, this study showed there is: a linear relation between increased serum lipid level and oxidative stress (TBARS Level); a linear relation between TBARS and HbA1c levels; and a reverse relation between TAS and HbA1c. We suggest that the increase in oxidative stress level in diabetics in general and specially in hyperlipidemic diabetics lead in part to increased HbA1c level away from serum glucose levels. The TAS levels indicate to importance of antioxidant vitamins, in particular vitamins E and C, in decreasing oxidative stress level, thus in decreasing HbA1c levels in diabetics. |
| المقدمة Introduction |
يتشكل الهيموغلوبين الغلوكوزي Glycated
Hemoglobin (HbA1c) نتيجة عدة تفاعلات لا إنزيمية متسلسلة بين الهيموغلوبين والغلوكوز في الدم, وتشير الدراسات إلى وجود علاقة خطية طردية قوية بين مستويات HbA1c ومستويات غلوكوز الدم, وشكلت هذه القاعدة حجر الأساس في الاعتماد على مستويات الهيموغلوبين الغلوكوزي لمعرفة واقع مستويات غلوكوز الدم عند المرضى السكريين لفترة تسبق 6-8 أسابيع من يوم الاختبار, وبذلك أصبحت معايرة HbA1c جزءاً هاماً من اختبارات التشخيص المخبري للداء السكري (2، 10، 14).
تؤكد الدراسات الأخيرة أن الهيموغلوبين الغلوكوزي هو أحد نواتج إدخال الغلوكوز النهائية المتقدمة (AGE) Advanced Glycation end- products, ونواتج الأكسدة المتقدمة للبروتينات (AOPP) Advanced oxidation protein products, التي تتورط فيها الجذور الحرة وتفاعلاتها التأكسدية المؤذية للمكونات الحيوية. ومن هنا ظهر مصطلح "إدخال الغلوكوز التأكسدي Oxidative Glycation" الذي أصبح جزءاً هاماً في نشؤ الاختلاطات المرافقة للداء السكري بما في ذلك الأمراض القلبية الوعائية Cardiovascular Diseases (C.V.D), وآفات الأوعية الدقيقة والاعتلال الكلوي السكري (1، 3، 6، 8، 11، 17).
تزداد من جانب آخر، شدة إدخال الغلوكوز التأكسدي في الداء السكري بزيادة توليد الجذور الحرة, أو زيادة شدة الإجهاد التأكسدي Oxidative stress, بخاصة عند النمط II بسبب عدة عوامل أهمها: اضطراب مستويات شحميات الدم, وأيضاً كما بينت دراسات حديثة عديدة ازدياد تحرير الحديد من الهيموغلوبين الحاوي على الغلوكوز, حيث يسهم هذا الحديد في زيادة توليد الجذور الحرة وبالتالي تزداد وتيرة تفاعلات الأكسدة الفائقة وشدة الإجهاد التأكسدي (1، 4، 13، 14).
بناء على ما سبق فإننا نجد سكريين مفرطي شحميات الدم، وهم الأكثرية، وسكريين أسوياء شحميات الدم, واستناداً إلى أحدث الدراسات يزداد LDLg البروتين الشحمي خفيض الكثافة الحاوي على الغلوكوز عند السكريين وتنخفض لديهم مقاومة LDL للأكسدة المحرضة بالمعادن (أي بالجذور الحرة) مما قد يسهم في ازدياد سوء وظيفة بطانة الأوعية عندهم (5، 12، 18). إضافة إلى ما سبق هناك مؤشرات أخرى ترفع من اختطار الإصابات القلبية الوعائية عند السكريين، وأمثلة ذلك:
أولاً: تزداد في الداء السكري نسبة LDL(s), البروتين الشحمي خفيض الكثافة, طرداً مع ازدياد مستويات كل من HbA1c وغلوكوز الدم والكوليستيرول وثلاثيات الغليسريد (T.G) وأيضاً طرداً مع LDLx (LDL المؤكسد), كما يتناسب LDL(s) عكساً مع مستويات HDL (5، 9، 10، 18).
ثانياً: تتناقـص عند المرضى السـكريـين
مجمل مستويات مضادات التأكسد (TAS) Total Antioxidant Status في البلازما مما يزيد من إمكان ازدياد أكسدة LDL, الأمر الذي يعد الحلقة الأساسية في تشكيل العصيدة الشريانية, وتشير الدراسات هنا إلى وجود علاقة خطية طردية واضحة بين درجة أكسدة LDL ومستويات HbA1c (1، 3، 6، 11، 13، 15).
استناداً إلى ما سبق توجهنا في بحثنا هذا إلى دراسة العلاقة بين مستويات الهيموغلوبين الغلوكوزي وشدة الإجهاد التأكسدي عند مرضى الداء السكري من النمط الثاني مفرطي وأسوياء شحميات الدم بهدف الإجابة عن الأسئلة التالية:
1- هل تُعبِّر مستويات HbA1c فقط عن مستوى سكر الدم عند مرضى السكري لفترة سابقة بـ 6-8 أسابيع؟
2- هل يمكن أن يكون الإجهاد التأكسدي مسؤولاً بشكل جزئي عن ازدياد مستوى HbA1c بغض النظر عن مستوى سكر الدم؟
|
| المواد والطرق Materials and Methods |
توزع الأفراد الذين خضعوا للدراسة على الفئات التالية:
1- فئة المراقبة (25 فرداً) – أفراد أصحاء تماماً لا يشـكون من أي مرض، أسـوياء
شحميات الدم بمتوسط عمر 48 عاماً.
2- فئة التجربة (25 فرداً) مرضى سكريين من النمط II بمتوسط عمر 49 عاماً وقد توزعوا كأسوياء شحميات الدم ومفرطي شحميات الدم.
أجريت الاختبارات التالية على عينات الدم المأخوذة:
1- معايرة الغلوكوز والكوليستيرول الكلي (T.ch) و LDL-ch و HDL-ch وثلاثيات الغليسريد (T.G) في المصل باستخدام عتيدة عمل جاهزة من شركة Randox البريطانية.
2- معايرة الهيموغلوبين الغلوكوزي في الدم المأخوذ على مانع التخثر EDTA بطريقة الاستشراب على عمود تبادل هابطي Colum chromatography cation exchange بعتيدة عمل جاهز من شركة Biosystem الأسبانية.
3- معايرة مضادات التأكسد الإجمالية في البلازما Total antioxidant status (TAS) باستخدام عتيدة عمل جاهزة من شركة Randox البريطانية.
4- معايرة المواد المتفاعلة مع حمض التيوباربيتوريك (TBARS) Thiobarbituric acid reactive substances في المصل كمشعر تشخيص معتمد بحثياً لقياس درجة الإجهاد التأكسدي وشدة تفاعلات الجذور الحرة (7، 16)، حيث يعتمد مبدأ المعايرة على تشكيل معقدات لونية بين نواتج تفاعلات الأكسدة الفائقة للشحميات وبين حمض التيوباربيتوريك وتستخلص هذه المعقدات بالبوتانول وتقاس كثافتها ثم يحسب التركيز استناداً إلى مخططات معيارية.
5- تمت معالجة النتائج إحصائياً واستنتاج العلاقة P وفق جدول ستيودنت بمقارنة فئة التجربة مع فئة المراقبة, ومقارنة السكريين مفرطي شحميات الدم مع السكريين أسوياء شحميات الدم.
|
| النتائج Results |
عرضت النتائج في الجدول 1 كمتوسط حسابي للمتغيرات المدروسة مع الانحراف المعياري X ± SD في فئتي التجربة والمراقبة. وقد كانت لمعظم النتائج اختلافات وعلاقات P ضمن مجال الثقة.
نرى أن قيم المتغيرات المدروسة في فئة المراقبة تقع ضمن المجالات السوية للأفراد الأصحاء, وبمقارنة هذه النتائج مع نتائج فئة التجربة السكريين (كل المرضى) نلاحظ وجود ازدياد واضح في نتائج السكريين كنسبة مئوية باعتبار فئة المراقبة 100% كما يلي:
الغلوكوز +118%, HbA1c +64%, T.ch +15%, LDL-ch +20%, HDL-ch +2%, T.G +45%, TBARS +27%, في حين انخفضت مستويات TAS عند السكريين بنسبة -22% .
وبمقارنة نتائـج فئة المراقبـة مع نتـائـج
السكريين أسوياء شحميات الدم نجد أن مستويات الغلوكوز قد ازدادت بنسبة +114% و HbA1c +56% و T.ch +2% و LDL-ch +3% و T.G +8% و TBARS +20% وانخفضت مستويات HDL-ch بنسبة -1% ومستويات TAS بنسبة -20% ودوماً بالمقارنة مع فئة المراقبة (100%), ونرى من هذه النتائج انه لا توجد اختلافات تقريباً في مستويات شحميات الدم بين فئتي المراقبة والسكريين أسوياء شحميات الدم.
أما عند مقارنة نتائج فئة المراقبة مع نتائج السكريين مفرطي شحميات الدم فنجد أن مستويات الغلوكوز قد ازدادت بنسبة +121%, HbA1c +72% و T.ch +30% و LDL-ch +38%, HDL-ch +5% و T.G +80% و TBARS +32%, أما مستويات TAS فقد انخفضت بنسبة -24% ونلاحظ انه توجد اختلافات واضحة في مستويات شحميات الدم (T.G, LDL-ch, T.ch) بين فئتي المراقبة والسكريين مفرطي الشحميات.
كما تم مقارنة نتائج السكريين مفرطي الشحميات مع السكريين أسوياء شحميات الدم ووجدنا أنه تزداد عند السكريين مفرطي شحميات الدم كل من الغلوكوز بنسبة 3%, HbA1c +11%, T.G +28.7%, LDL-ch 34.6%, HDL-ch +7.5%, T.G +72.6%, TBARS +9.5%, وتنخفض عندهم TAS بنسبة -5% وذلك بالمقارنة مع السكريين أسوياء شحميات الدم.
|
الجدول 1: المتوسط X ± SD للمتغيرات المدروسة عند فئات التجربة والسكريين نمط II.
الفئة |
غلوكوز
ملغ/د.ل
110-70 |
HbA1c
%upTo 8 |
T.ch
ملغ/د.ل
Up to
160 |
LDL
ملغ/د.ل
Up to
160 |
HDL
ملغ/د.ل
Up to
35-45 |
T.G
ملغ/د.ل
Up to
150 |
TAS
ممول/ل
1.75-1.3 |
TBARS
مكمول/ل |
المراقبة |
108.12±
19.34 |
5.8 ±
0.66 |
195.72±
12.99 |
138.28±
10.55 |
39.6 ±
5.5 |
115.36±
24.02 |
1.52 ±
0.1 |
4.736 ±
0.32 |
سكريون |
235.12± ** 44 |
9.5 ±
** 1.18 |
225.4 ± * 32.8 |
166.2 ± * 27.16 |
40.24 ± * 5.6 |
167 ± * 52.8 |
1.18 ± ** 0.07 |
6.0 ± ** 0.41 |
سكريون أسوياء الشحميات |
231.5 ± ** 38.6 |
9.05 ± ** 0.54 |
198 ± * 13.2 |
142.5 ± * 10 |
38.85 ± * 3.5 |
124.1 ± * 22.82 |
1.21 ± ** 0.64 |
5.7 ± ** 0.32 |
سكريون مفرطو الشحميات |
239.1 ± ** 50.7 |
10 ± ** 1.5 |
255.2 ± ** 17.5 |
191.8 ± ** 11 |
41.75 ± * 7.1 |
214.1 ± ** 31.5 |
1.15 ± ** 0.06 |
6.24 ± ** 0.30 |
P * > 0.05
** P < 0.05 وذلك بالمقارنة مع فئة المراقبة.
|
| المناقشة Discussion |
| يبين الشكل 1 وجود علاقة خطية طردية بين مستويات الغلوكوز والهيموغلوبين الغلوكوزي وهذا كما ذكرنا سابقاً هو الأساس في الاعتماد على معايرة مستوى HbA1c في التشخيص المخبري للداء السكري, وهو يشير بوضوح إلى دور مستويات غلوكوز الدم في عملية غلكزة هيموغلوبين الدم وتشكيل HbA1c, من جانب آخر يبين الشكل 2 وجود علاقة خطية طردية واضحة بين مستوى غلوكوز الدم وكمية TBARS في المصل أي انه بزيادة مستوى غلوكوز الدم تزداد شدة الإجهاد التأكسدي (2، 4). وهذا يعود إلى عدة عوامل أهمها: ارتفاع مستويات شحميات الدم عند السكريين وازدياد تحرير الحديد المؤكسد وانخفاض مستويات مضادات التأكسد الإجمالية في الدم وهذا ما يؤكده الشكل 3 الذي يبين لنا وجود علاقة خطية طردية بين مستويات TBARS و LDL-ch أي أنه عند زيادة مستويات LDL-ch تزداد نواتج الأكسدة الفائقة للشحميات وشدة الإجهاد التأكسدي (5، 9، 10). وهذا يشير أيضاً إلى ازدياد أكسدة LDL عند السكريين عموماً وعند مفرطي الشحميات منهم على وجه الخصوص, كما أنه بزيادة مستويات T.G (الشكل 4) تزداد أيضاً شدة الإجهاد التأكسدي لأن ازدياد T.G يكون باعثاً على ازدياد تشكيل LDL(s)، الذي يتميز بانخفاض قابليته للأكسدة المتواسطة بالجذور الحرة فتزداد بالتالي تفاعلات الأكسدة الفائقة للشحميات. نرى من الشكل 5 وجود علاقة خطية طردية بين شدة الإجهاد التأكسدي (كمية TBARS) ومستويات الهيموغلوبين الغلوكوزي مما يشير إلى أنه بزيادة توليد الجذور الحرة عند السكريين وزيادة تفاعلات إدخال الغلوكوز التأكسدية تزداد مستويات HbA1c (1، 6)، وإذا قمنا بمقارنة نتائج المتغيرات المدروسة بين السكريين مفرطي شحميات الدم وأسوياء شحميات الدم (ويمكن اعتبار أسوياء شحميات الدم هنا كمراقبة) نلاحظ أنه ومع عدم وجود اختلاف يذكر بمستويات غلوكوز الدم بين السكريين مفرطي وأسوياء شحميات الدم (+3% عند السكريين مفرطي شحميات الدم), فإننا نجد أن مستويات الهيموغلوبين الغلوكوزي عند السكريين مفرطي الشحميات أعلى بـ 11% مما عند السكريين أسوياء الشحميات الدم؛ وبالوقت ذاته نجد أن الإجهاد التأكسدي عند السكريين مفرطي شحميات الدم أكثر شدة بـ 10% مما عند السكريين أسوياء الشحميات الدم. ويمكننا القول أن هذا الاختلاف بشدة الإجهاد التأكسدي يعود للاضطراب الواسع في مستويات شحميات الدم عند السكريين مفرطي شحميات الدم، وهذا يؤدي بدوره إلى ازدياد تشكيل الهيموغلوبين الغلوكوزي بغض النظر عن مستوى غلوكوز الدم, ومما يسهم في هذا أيضاً انخفاض مستوى TAS عند السكريين عموماً وبخاصة عند السكريين مفرطي شحميات الدم مقارنة مع أسوياء شحميات الدم، الأمر الذي يشير إلى أهمية إدخال الفيتامينات مضادات التأكسد (6)، خاصة الفيتامينات C, E ضمن العلاج المعطى للسكريين، لأنه وكما يبين الشكل 6 توجد علاقة بين مستويات TAS ومستوى HbA1c. |
| الاستنتاج Conclusions |
| نقترح أن ارتفاع مستويات الهيموغلوبين الغلوكوزي عند السكريين النمط II ناجم بشكل رئيسي عن ارتفاع مستويات غلوكوز الدم وبشكل جزئي عن ارتفاع شدة الإجهاد التأكسدي وانخفاض مستويات TAS عند السكريين وخاصة مفرطي الشحميات منهم, ويمكن بالمقابل أن يشير ارتفاع مستويات HbA1c إلى ارتفاع شدة الإجهاد التأكسدي وازدياد تعرض LDL للأكسدة وبالتالي إلى
ازدياد خطر الإصابات القلبية الوعائية عند السـكريين عموماً ويمكن أن يؤدي إعطـاء جرعات من الفيتامينات مضادة التأكسد C, E للسكريين إلى تخفيض جزئي في تشكل وفي مستويات HbA1c عند السكريين وبالتالي الحد من تحرير الحديد المحرض على تشكيل الجذور الحرة والحد من شدة الإجهاد التأكسدي.
|
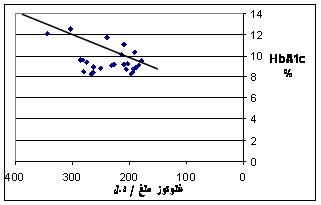
الشكل 1: العلاقة بين الغلوكوز و HbA1C.
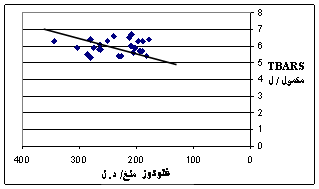
الشكل 2: العلاقة بين الغلوكوز و TBARS.
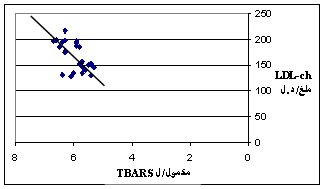
الشكل 3: العلاقة بين LDL-ch و TBARS.
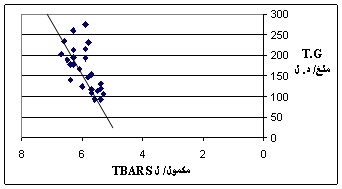
الشكل 4: العلاقة بين T.G و TBARS.
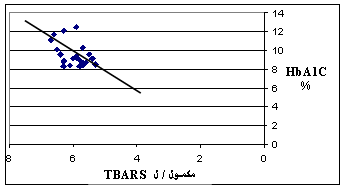
الشكل 5: العلاقة بين HbA1C و TBARS.
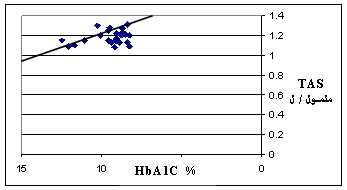
الشكل 6: العلاقة بين TAS و TBARS. |
| المراجع References |
1-Abou- Seif MA. and Youssef AA.
Evaluation of some biochemical changes in diabetic patients.
Clin. Chim Acta. 16; 346(2), 2004.
2-Ahmed N; Baboei- Jadidi R. et al.
Degradation products of proteins damaged by glycation, oxidation and nitration in clinical type 1 diabetes.
Diabetologic. 48(8), 2005.
3-Dursun E; Timur M. et al.
Protein oxidation in type 2 diabetic patients on hemodialysis.
J. Diabetes Complications. 19(3), 2005.
4-Greismacher A; Kindhauser M. et al.
Enhanced serum levels of TBARS in diabetes mellitus.
Am. J. Med. (5), 1998
5-Guerei B; Antebi H. et al.
Increased ability of LDL from normolipidemic Type 2 diabetic women to generate peroxides.
Clin. Chem. 45(9), 1999.
6-Halliwell B. and Gutteridage J.
Free Radicals in biology and medicine.
M.C.Oxford University Press. 1999.
7-Janero D.R.
Malondialdehyde and thiobarbituric acid reactivity substances as diagnosis indices of lipid peroxidation and peroxidative tissue
injury.
Free Radic. Biol. Med. 9, 1999.
8-Kalousova M; Skrha J. and Zima T.
Advanced glycation end- products and advanced oxidation protein products in patients with diabetes mellitus.
Physiol Res. 51 (6), 2002.
9-Lee W; Min WK; Chun S; Jang S. et al.
Low- density lipoprotein subclass and its correlating factors in diabetics.
Clin. Biochem. 36(8), 2003.
10-Mac Donald- Wicks L; Gibson LZ. et al.
Oxidised LDL in newly diagnosed Type 2 diabetes mellitus and impaired glucose Tolerance.
Asia Pac J. Clin Nutr. 13, 2004.
11-McCusKer CA; Lamont JV. and Fitz Gerald SP.
Total antioxidant status and Lipid peroxidation in diabetic patients. TAS studies.
Randax Lab. IID, UK, RIT2. 11, 1995.
12-Neyestani TR; Alipour- Birgani R. et al.
Glycemic optimization may reduce lipid peroxidation independent of weight and blood lipid changes in Type 2 diabetes mellitus.
Diabetes Nutr. Metal. 17(5), 2004.
13-Pieri C; Testa R; Marra; Bonfigli AR; Manfrini S. and Testa I.
Age- dependent changes of serum oxygen radical scavenger capacity and haemoglobin glycosylation in non- insulin – dependent diabetes mellitus.
Gerontology. 47(2), 2001.
14-Sen S; Kar M; Roy A, and Chakraborti AS.
Effect of nonenzymatic glycation on functional and structural properties of hemoglobin.
Biophys. Chem.. 1; 113(3), 2005.
15-Vessby J; Basu S; Mohsen R; Berne C. and Vessby B.
Oxidative stress and antioxidatnt status in type I diabetes mellitus.
J Inter Med. 251(1), 2002.
16-Wasowicz W; Neve J. and Peretz A.
Optimized steps in fluorometric determination of thiobarbituic acid reactive substances in serum.
Clin. Chem. 3, 1993.
17-Wautier JL. and Schmidt AM.
Protein glyation: afirm link to endothelial cell dysfunction.
Circ. Res. 6; 95(3), 2004.
18-Wen Y; skidmopre JC; Porter – Turner MM. et al.
Rrelationship of glycation, antioxidant status and oxidative stress to vascular endothelial damage in diabetes.
Diabetes obes. Metab. 4(5), 2002
|
| المجلد 4 ,
العدد 3
, رمضان 1427 - تشرين الأول (أكتوبر) 2006 |
|
|
|
