| المجلد 4 ,
العدد 8
, ذو الحجة 1428 - كانون الثاني (يناير) 2008 |
| |
| العلاج بـ Sandostatin-LAR عند مرضى ضخامة النهايات |
| Treatment with Sandostatin-LAR in Patients with Acromegaly |
| د. نجات صنيج، كلية الطب، جامعة دمشق |
| Najat SNEIGE |
| Damascus University, Faculty of Medicine |
| الملخص Abstract |
يدور البحث حول دراسة مستقبلية لتقييم تأثير العلاج الدوائي بـSandostatin-LAR (Long-acting repeatable)، شملت الدراسة 7 مرضى ضخامة نهايات خضعوا جميعاً للعمل الجراحي على الغدة النخامية لاستئصال الورم المفرز لهرمون النمو، لم تحقق الجراحة الاستجابة (تعرف الاستجابة للجراحة بعودة قيم الـ IGF-1 إلى الحدود الطبيعية وتثبيط الـ GH بعد 100 غ غلوكوز إلى أقل من 2 ng/ml).
أظهرت هذه الدراسة نقصاً بقيم الـ IGF-1 والـ GH على الأقل 27%، 67.5% على التوالي مقابل القيم الأساسية بعد علاج قصير الأمد بالدواء المذكور أعلاه للمرضى السبعة، أعطي الـ Sandostatin-LAR بجرعة 10 ملغ عضلياً كل 28 يوماً ولمدة 3 أشهر.
أبدت القيمة الوسطية لـ IGF-1 نقصا ً واضحاً عند المرضى السابقين من 641.85 ng/ml إلى 467.85 ng/ml (p<0.05).
القيمة الوسطية للـ GH لدى المرضى انخفضت من 32.40 ng/ml إلى 10.5 ng/ml (p<0.05) بعد العلاج الدوائي لمدة 3 أشهر. مريض واحد من المرضى السابقين عادت لديه قيمة كلٍ من الـ IGF-1 والـ GH بعد التثبيط بالغلوكوز إلى القيم الطبيعية، ومريض أخر لم يحقق استجابة فكانت قيم IGF-1 قبل العلاج الدوائي 638 ng/ml وبعد العلاج ولمدة 3 أشهر 662 ng/ml، أما قيمة GH فكانت قبل العلاج 43.2 وبعد العلاج 43 ng/ml.
لم يشكو المرضى من تأثيرات جانبية ناجمة عن الدواء.
أما بالنسبة لحجم الورم فلم يلاحظ خلال هذه الفترة القصيرة وبالمتابعة بالمرنان للغدة النخامية أي تراجع لحجم الورم.
إن التراجع الواضح في القيم الوسطية لكلٍ من الـ GH بعد التثبيط والـ IGF-1 قبل العلاج وبعده خلال فترة قصيرة (3 أشهر) بـ Sandostatin-LAR يدعم دوره العلاجي لمرضى ضخامة النهايات وعلى الأقل لدى بعض المرضى.
|
The A respective Study evaluated the effects of treatment with Sandostatin-LAR (Long-acting repeatable) in patients with acromegaly. This study included 7 patients with acromegaly, and showed a reduction in IGF-1 and GH levels of at least 27% and 67.5% respectively vs. baseline levels after a short term (3 month) treatment. Sandostatin-LAR was given as 10 mg injection (I.M.) every 28 d for 3 injections, all patients had been operated to excise the GH- secreting pituitary adenoma, but surgery wasn’t curable. Mean value of IGF-1 showed significant reduction under the treatment from 641.85 to 467.85 ng/ml (p<0.05), and mean value of GH showed significant reduction from 32.40 ng/ml to 10.5 ng/ml (p<0.05). One patient didn’t respond to medical therapy, and in another patient the values of IGF-1 and GH returned toward normal range. The patients didn't complain from any important side effects of the drug.
No significant tumor shrinkage was observed during the short duration of the treatment. The predictive value of short-term results support the role of Sandostatin-LAR in the treatment of acromegaly as second line treatment after unsuccessful Surgery in at least some patients
|
| المقدمة Introduction |
ضخامة النهايات مرض مزمن مخاتل ينجم عن فرط إفراز الـ GH مع ارتفاع مستوى IGF-1 ويترافق مع زيادة معدل الإمراضيات والوفيات ويعود هذا غالباً إلى المرض الوعائي القلبي (1، 2). أظهرت الدراسات الوبائية أن زيادة معدل الوفيات المترافق مع ضخامة نهايات فعال يتراجع إلى المعدلات الطبيعية لدى المرضى الذين تحقق عندهم مستويات GH آمنة (GH< 2.5 ng/ml) ويكون هذا بغض النظر عن المقاربة العلاجية المطبقة (3-5).
عادة ما يكون الخط الأول في العلاج لهؤلاء المرضى عند الجراحين هو الجراحة؛ ويستعمل العلاج الدوائي أو يطبق لإنقاص الإفراز الزائد للـ IGF-1 وGH لدى مرضى غير ملائمين أو رفضوا الجراحـة أو بعد فشـل الجراحة، أو في حالات انتقائية كعلاج بدئي.
إن مضاهئات (SA) Depot Somatostatin analogs مثل Sandostatin-LAR يعطى عضلياً كل 28 يوماً وهو قادر على إنقاص فرط الإفراز الهرموني لدى غالبية المرضى وإعادة مستويات الـ IGF-1 إلى الطبيعية لدى العديد منهم.
يتحرر Sandostatin-LAR ببطء إلى الدوران ويحافظ على تثبيط مطول (28 يوم) لإفراز الـ IGF-1 والـ GH.
الهدف من هذه الدراسة هو تقييم تأثيرات العلاج بـ Sandostatin-LAR الطويل الأمد على مستويات الـ IGF-1 والـ GH، وعلى حجم الورم النخامي المفرز للـ GH لدى 7 مرضى ضخامة نهايات خضعوا للعمل الجراحي على الغدة النخامية دون استجابة.
كما تم تقييم تأثير هذا العلاج الدوائي على الأعراض السريرية والتظاهرات الشعاعية.
|
| المواد والطرق Materials and Methods |
شملت الدراسة 7 مرضى ضخامة نهايات (4 ذ كور، 3 إناث) بعمر 18-54 سنة (وسطياً 33.8 سنة)، وهي دراسة مستقبلية، قيّم فيها المرضى قبل بدء العلاج الدوائي بـ Sandostatin-LAR وبعد 3 أشهر منه وبجرعة 10 ملغ/ شهرياً ولمدة 3 أشهر.
خضع المرضى السابقون كلهم للعمل الجراحي لاستئصال ورم الغدة النخامية المفرز للـ GH مع استمرار فعالية الورم بعد الجراحة سريرياً ومخبرياً، لم يتثبط الـ GH إلى أقل من 2 ng/ml بعد إعطاء 100 غ غلوكوز فموي، وكذلك لم تعد قيم الـ IGF-1 إلى المستوى الطبيعي بما يناسب العمر الزمني. في حين أنه تحت العلاج الدوائي ومقارنة مع القيم الأساسية لـ GH حدث نقص بمقدار 67.5% ونقص بمقدار 27% لـ IGF-1 بعد 3 أشهر من العلاج بـ Sandostatin-LAR بجرعة 10 ملغ بفواصل 28 يوم (3 حقن).
تمت متابعة المرضى سريرياً أثناء فترة العلاج من ناحية الصداع، نمل وخدر، تعرق، تورم، تعب، آلام مفصلية، وشخير، كما توبع المرضى من حيث وجود تأثيرات جانبية للدواء.
تم جمع عينات الدم في الصباح الباكر.
- تمت مقايسة هرمون النمو على الريـق
وبعد ساعة من إعطاء 100 غ غلوكوز، كما تمت مقايسة IGF-1.
- تمت مقايسة GH بطريقة RIA، و IGF-1 بطريقة الـ Elisa micro (القيم الطبيعية هي 107- 310 ng/ml).
- أجري مرنان للغدة النخامية للمرضى كلهم قبل بدء العلاج الدوائي وبعد 3 أشهر على جهاز Tesla 1,5 closed.
- الطريقة الإحصائية اختبار per-test.
|
| النتائج Results |
تابع المرضى جميعهم العلاج بـ Sandostatin-LAR لمدة 3 أشهر، تحسنت الصورة السريرية لدى المرضى كلهم من صداع، تعب، ووهن عام، خدر ونمل، آلام مفصلية، تعرق، شخير.
أما من ناحية النتائج المخبرية: كان للـ Sandostatin-LAR تأثير واضح ومهم إحصائياً على تثبيط مستويات GH بعد 3 أشهر من العلاج. انخفضت القيمة المتوسطة الأساسية لـ GH من 32.40 ng/ml إلى 10.5 ng/ml بعد 3 أشهر من العلاج (p<0.05). (الشكل 1).
كذلك كان للعلاج تأثير واضح على قيم IGF-1 إذ كانت القيمة الوسطية الأساسية 641.85 ng / ml انخفضت إلى 467.85 ng/ml بعد 3 أشهر من العلاج (p<0.05). (الشكل 2).
- لم تلاحظ تأثيرات جانبية هضمية أو غيرها للدواء خلال الدراسة.
- لم يستجيب أحد المرضى للعلاج الدوائي بـ Sandostatin-LAR إذ كان GH الأساسي 43.22 ng/ml وبعد العلاج 43 ng/ml كما كان IGF-1 الأساسي 638 ml/ng وبعد العلاج 622 ng/ml.
- بالمقابل مريض واحد من المرضى السبعة عادت القيم المخبرية لديه طبيعية فكان GH الأساسي 34 ng/ml وبعد المعالجة أصبح 0.33 ng/ml وكذلك IGF-1 كان أساسياً 542 ng/ml وأصبح 100ng/ml بعد العلاج.
- بالنسبة للمتابعة الشعاعية بالمرنان، لم يلاحظ زيادة في حجم الورم لدى أي مريض كما لم يلاحظ تراجع في حجم الورم لدى أي منهم.
- لم ينسحب أي مريض من الدراسة بسبب تأثيرات جانبية لـ Sandostatin-LAR فلم يلاحظ أي تأثير جانبي له سواء هضمي (نفخة، إقياء، غازات)، ولم يحدث ألم موضعي مكان الحقن، ولم تلاحظ تبدلات كيميائية حيوية أو دموية بالتحاليل الروتينية.
|
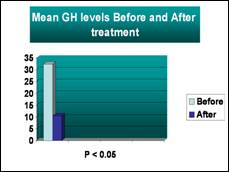
الشكل 1: متوسط مستويات GH قبل المعالجة وبعدها.

الشكل 2: متوسط مستويات IGF-1 قبل المعالجة وبعدها.
|
| المناقشة Discussion |
إن نتائج الدراسات التي قيمت علاج ضخامة النهايات بمضاهئات analogs الـ Somatostatin مثل Sandostatin-LAR دعمت استعمال مثل هذه العوامل الدوائية كعلاج دوائي بدئي (6-8) أو بعد العمل الجراحي على الورم النخامي في حال عدم الاستجابة (9-11).
والعلاج المثالي لضخامة النهايات هو الذي يعيد إفراز GH إلى القيم الطبيعية (12) محققاً مستويات IGF-1 طبيعية وقادراً على ضبط نمو الورم وإنقاص حجمه محرراً الغدة النخامية من ضغط الكتلة الورمية محافظاً على وظائفها الأخرى مع القدرة على تحمل هذا الدواء (13).
إن إدخال العلاج بمضاهئات Somatostatin
مثل Sandostatin-LAR (14-17) ذي نصف العمر القصير جداً، كان ثورة حقيقية في علاج مرضى ضخامة النهايات حيث أنه من الصعب جداً استئصال مثل هذه الأورام بشكل كامل نظراً لأهمية مجاوراتها التشريحية؛ لذلك بتوفر مثل هذه الأدوية أصبح هناك أمل بضبط هذه الأورام ريثما تبدأ فعالية العلاج الشعاعي الذي يحتاج إلى 7- 10 سنوات على الأقل، حيث أن ثلاثة من مرضانا كان قد طبق لديهم العلاج الشعاعي وذلك قبل فترة قصيرة من البدء بالعلاج الدوائي لديهم. وحديثاً طورت مضاهئات السوماتوستاتين طويلة الأمد في عملها (حتى 14-28 يوماً) وهما Lanreotide وOctereotide-LAR وتبقى مشكلة هذه الأدوية هي غلاء ثمنها (18-25).
إن Sandostatin-LAR أي Octreotide-LAR وهو الذي طبق لدى مرضانا، قادر على خفض فرط إفراز GH بحقن شهرية محققاً مستويات آمنة من GH في 56% من المرضى ويعيد IGF-1 إلى الطبيعي في 66% حسب نتائج Freda (16) و Was (26) و Ezzat (27)، أما نتائجنا فقد أثبتت فعالية Octreotide-LAR في ضبط الإفراز الهرموني لدى مرضى ضخامة النهايات غير
المستجيبين للعمل الجراحي.
فمرضانا استجابوا للعلاج ولكن بشكل جزئي إذ أظهروا نقصاً في مستويات GH 67.5% مقارنة مع القيم الأساسية ومقارنة مع دراسة Renato (28) نجد أن نتائجه متماشية مع نتائج دراستنا إذ أن القيمة المتوسطات للـ GH انخفضت من 2.4-20.7 ng/ml أساسياً إلى 0.5-3.6 ng/ml بعد 3 أشهر، وIGF-1 هبط من 26-776 ng/ml إلى 19- 379 ng/ml بعد 3 أشهر.
- وكثير من الدراسات المطولة الأمد أظهرت لسنوات أن مستويات IGF-1 /GH بعد 3 أشهر من العلاج الدوائي في الواقع هي المنبئ الأفضل بالنتائج النهائية للعلاج الطويل الأمد (29، 30).
- أبدت كثير من الدراسات (31-33) تراجع حجم الورم (46%) من المرض، ولكنها كانت دراسات لفترة طويلة. هذا الشيء لم يلاحظ في دراستنا، وهذا يعود إلى قصر فترة العلاج وعلى الرغم من عدم التراجع الشعاعي كان هناك تراجعاً مخبرياً ويعود هذا إلى التأثير المضاد للتكاثر الخلوي للـ Octereotide-LAR.
|
| الاستنتاج Conclusion |
|
لاحظنا في دراستنا استجابة جزئية في سلسلة مرضانا من الناحية المخبرية دون تراجع حجم الورم، وينوه هذا إلى الحاجة إلى مقايسة دقيقة للعلاج لكل من الجرعة والوقت للحصول على نتائج مثالية. أي رفع جرعة الدواء إلى 20-30 ملغ مع إطالة فترة العلاج(34) .
|
| المراجع References |
1-Wright AD, Hill DM, Lowy C. and
Fraser TR.
Mortality in acromegaly.
Q J Med; 39: 1-16, 1970.
2-Rajasoorya C, Holdaway IM, Wrightson P, Scott DJ. and Ibbertson HK.
Determinants of clinical outcome and survival in acromegaly.
Clin Endocrinol (Oxf), 41: 95-102. 1994.
3-Bates AS, Van’t Hoff W, Jones JM. and Clayton RN.
An audit of outcome of treatment in acromegaly.
Q J Med; 86: 293-299, 1993.
4-Melmed S, Jackson I, Kleinberg D. and Klibanski A.
Current treatment guidelines for acromegaly.
J Clin Endocrinol Metab; 83: 2646-2652, 1998.
5-Melmed S. et al.
For the Acromegaly Treatment Consensus Workshop Participants.
Guidelines for acromegaly management.
J Clin Endocrinol Metab; 87: 4054-4058, 2002.
6-Newman CB. et al.
Octreotide as primary treatment for acromegaly.
J Clin Endocrinol Metab; 83: 3034-3040, 1998.
7-Pedroncelli AM, Montini M, Gianola D, Pagani MD, Albani G, Dallabonzana D. and Pagani G.
Octreotide LAR as first line therapy in acromegaly: preliminary results [Abstract OC16].
Pituitary, 3: 20, 2000.
8-Colao A. et al.
The effects of octreotide-LAR
given as first line therapy in patients with acromegaly.
10th Meeting of the European Neuroendocrine Association, Munich, Germany, PB-308, 141, 2002.
9-Lissett CA, Peacey SR, Laing I, Tetlow L, Davis JR. and Shalet SM.
The outcome of surgery for acromegaly: the need for a specialist pituitary surgeon for all types of growth hormone (GH) secreting
adenoma.
Clin Endocrinol (Oxf), 49: 653-657, 1998.
10-Gittoes NJ, Sheppard MC, Johnson AP. and Stewart PM.
Outcome of surgery for acromegaly: the experience of a dedicated pituitary surgeon.
Q J Med; 92: 741-745, 1999.
11-Laws ER, Vance ML. and Thapar K.
Pituitary surgery for the management of acromegaly.
Horm Res; 53 (3): 71-75, 2000.
12-Giustina A, Barkan A, Casanueva FF, Cavagnini F, Frohman L, Ho K, Veldhuis J, Wass J, Von Werder K. and Melmed S.
Criteria for cure of acromegaly: a consensus statement.
J Clin Endocrinol Metab; 85: 526-529, 2000.
13-Newman B. et al.
Safety and efficacy of long- term octreotide therapy of acromegaly: results of a multicenter trial in 103 patients: a clinical research center study.
J Clin Endocrinol Metab; 80: 2768-2775, 1995.
14-Giusti M, Gussoni G, Cuttica CM.
and Giordano G.
Effectiveness and tolerability of slow release lanreotide treatment in active acromegaly: six-month report on an Italian multicenter study.
J Clin Endocrinol Metab; 81: 2089-2097, 1996.
15-Stewart PM, Kane KF, Stewart SE, Lancranjan I. and Sheppard MC.
Depot long-acting somatostatin analog (Sandostatin LAR) is an effective treatment for acromegaly. J Clin Endocrinol Metab; 80: 3267-3272. 1995.
16-Freda PU.
Somatostatin analogs in acromegaly.
J Clin Endocrinol Metab; 87: 3013-3018, 2002.
17-Gillis JC, Noble S. and Goa KL.
Octreotide long-acting release (LAR). A review of its pharmacological properties and therapeutic use in the management of acromegaly.
Drugs, 53: 681-699, 1997.
18-Bauer W. et al.
SMS 201-995: a very potent and selective octapeptide analogue of somatostatin with prolonged action.
Life Sci; 3: 1133-1140, 1982.
19-Lamberts SWJ, Uitterlinden P. and Del Pozo E.
SMS 201-995 induces a continuos decline in circulating growth hormone and somatomedin-C levels during therapy of acromegalic patients for over two years.
J Clin Endocrinol Metab; 65: 703-710, 1987.
20-Vance ML. and Harris AG.
Long-term treatment of 189 acromegalic patients with the somatostatin analog octreotide. Results of the International Multicenter
Acromegaly Study Group.
Arch Intern Med; 151: 1573-1588, 1991.
21-Lancranjan J. et al.
Sandostatin-LAR: a promising therapeutic tool in the management of acromegalic patients.
Metabolism, 45: 67-71, 1996.
22-Flogstad AK, Halse J, Bakke S, Lancranjan J, Marbach P, Bruns Ch, Jervell J.
Sandostatin LAR in acromegalic patients: long-term treatment.
J Clin Endocrinol Metab; 82: 23-31, 1997.
23-Amato G. et al.
Long-term effects of lanreotide SR and octreotide LAR on tumour shrinkage and GH hypersecretion in patients with previously untreated
acromegaly.
Clin Endocrinol (Oxf), 56: 65-71, 2002.
24-Bevan JS. et al.
Primary medical therapy for acromegaly: an open, prospective, multicenter study of the effects of subcutaneous and intramuscular
slow-release octreotide on growth hormone, insulin-like growth factor-I, and tumor size.
J Clin Endocrinol Metab; 87: 4554, 4563, 2002.
25-Van der Lely AJ, Harris AG. and Lamberts SWJ.
The sensitivity of growth hormone
secretion to medical treatment in acromegalic patients: influence of age and sex.
Clin Endocrinol (Oxf), 37: 181-185, 1992.
26-Wass JAH.
Growth hormone, insulin-like growth factor-I and its binding proteins in the follow-up of acromegaly.
J Endocrinol, 155: S17-S19, 1997.
27-Ezzat S, Snyder PJ, Young WF, Boyajy LD, Newman C, Klibanski A, Molitch ME, Boyd AE, Sheeler L. and Cook DM.
Octreotide treatment of acromegaly: a randomized multicenter study.
Ann Intern Med; 117: 711-718, 1992.
28-Renato Cozzi، Roberto Attanasio, Marcella Montini Glovann, Lasio, Sandro Lodrini and Alberto M Pepronelli.
Four Year Treatment With Octreotide Long Acting Repeatable in acromegalic Patients: Predictive Value of Short- Term Results?
J Clin Endocrinol Metab, 88 (7): 3090-3098.
29-Colao A, Ferone D, Lastoria S, Marzullo P, Cerbone G, Di Sarno A, Longobardi S, Merola B, Salvatore M. and Lombardi G.
Prediction of efficacy of octreotide therapy in patients with acromegaly.
J Clin Endocrinol Metab; 81: 2356-2362, 1996.
30-John S Bevan.
The Antitumoral Effects of Somatostatin Analog Therapy in Acromegaly.
J Clin Endocrinol Metab; 90 (3): 1856-1863.
31-Colao A, Ferone D, Marzullo P, Cappabianca P, Cirillo S, Boerlin V, Lancranjan I. and Lombardi G.
Long-term effects of depot long-acting somatostatin analog octreotide on hormone levels and tumor mass in acromegaly.
J Clin Endocrinol Metab; 86: 2779-2786, 2001.
32-Cozzi R, Barausse M, Sberna M, Lodrini A, Franzini A, Lasio G. and Attanasio R.
Lanreotide 60 mg, a longer acting somatostatin analog: tumor shrinkage and hormonal normalization in acromegaly.
Pituitary, 3: 231-238, 2000.
33-Annamaria Colao.
Partial Surgical Removal of Growth Hormone-Secreting Pituitary Tumors Enhance the Respouse to Somatostatin Analogs in Acromegaly.
J clin Endocrinol Meab; 91 (1): 85-92.
34-Jenkins PJ, Akker S, Chew SL, Besser GM, Monson JP. and Grossman AB.
Optimal dosage interval for depot somatostatin analogue therapy in acromegaly requires individual titration.
Clin Endocrinol (Oxf), 53: 719-724, 2000.
|
| |
| المجلد 4 ,
العدد 8
, ذو الحجة 1428 - كانون الثاني (يناير) 2008 |
|
|
|
