| المجلد 5 ,
العدد 10
, المحرم 1432 - كانون ثاني (يناير) 2011 |
| |
| دراسة تراكيز الهيالورونان المصلية كواصم للاعتلال الوعائي
عند المرضى السكريين من النمط الثاني
|
| Study of Serum Hyaluronan Concentrations as a Marker of Angiopathy in Patients with Type II Diabetes Mellitus |
| د. سوزان سليمان، أ.د. إميل شاهين و أ.د. فايزة القبيلي |
| uzan Soulieman S., Chahine E. and Alquobaili F. |
كلية الصيدلة، جامعة دمشق، سورية
Faculty of Pharmacy, Damascus University |
| الملخص Abstract |
يترافق فرط سكر الدم السكري المزمن بضرر طويل الأمد، مع خلل وظيفي، وفشل أعضاء مختلفة، وخاصة العين، والكليتين، والأعصاب، والقلب والأوعية الدموية. يطرأ تبدل على استقلاب العديد من مكونات الجسم تحت تأثير فرط سكر الدم، بما فيها مكونات المطرس خارج الخلوي، حيث يعد الهيالورونان Hyaluronan (HA) المكون الرئيسي. ويسبب فَرْطُ سُكَّرِ الدَّم زيادة في تَخْليق HA. وأظهرت الدراسات الحديثة وجود زيادة إنتاج للهيالورونان في التصلب الشرياني المرتبط بالسكري واعْتِلاَلُ الكُلْيَة السكري.
جرت مقايسة المستويات المصلية للهيالورونان ومستويات الغلوكوز الصيامي وتراكيز الهيموغلوبين السكري لدى 87 شخصاً (23 أسوياء ظاهرياً، 32 مصاباً بالسكري من النمط الثاني بدون مضاعفات وعائية، 33 مريضاً بالسكري من النمط الثاني مع مضاعفات وعائية). اعتمد اختبار T student للتحليل الإحصائي، واعتمدت قيمة p<0.05 للإعتداد الإحصائي، واعتمد معامل person لتعيين الارتباط بين المتثابتات المدروسة.
أوضحت دراستنا أن مستويات هيالورونان المصل كانت أعلى بشكل يعتد به (p<0.001) لدى مرضى السكري من النمط الثاني (X±SD: 59.5±4.7 نغ/ مل) مقارنة مع المجموعة الشاهدة (X±SD: 36.9±4.4 نغ/ مل). كما وجدنا أيضاً أن المستويات المصلية للهيالورونان كانت أعلى بشكل يعتد به (p<0.001) لدى مرضى السكري الذين يعانون من المضاعفات السكرية الوعائية، بالمقارنة مع مجموعة مرضى السكري بدون مضاعفات وعائية والمجموعة الشاهدة (72.1±5.2، 59.5±4.7، 36.9±4.4 نغ/ مل، على الترتيب).
|
The chronic hyperglycemia of diabetes is associated with long-term damage, dysfunction, and failure of different organs, especially the eyes, kidneys, nerves, heart, and blood vessels. Hyperglycemia changes the metabolism of many body components, including the extra cellular matrix, where Hyaluronan (HA) is considered the main component. Hyperglycemia causes an increase in the synthesis of HA. Recent studies have reported an increase in HA production in diabetes-related arterial sclerosis and diabetic nephropathy.
Serum levels of HA and fasting glucose and the concentrations of glycosylated hemoglobin are measured in 87 subjects (23 normal persons, 32 patients of type 2 diabetes without vascular complications, and 33 patients of type 2 diabetes with vascular complications). T student test was used in the statistical analysis, p<0.05 of statistical significance, and Person coefficient for determination of studied parameters correlation.
Our study illustrated that serum levels of HA were significantly higher (p<0.001) in patients with type 2 diabetes (X±SD: 59.5±4.7 ng/ ml), compared with the control group (X±SD: 36.9±4.4 ng/ ml). serum levels of HA is also significantly higher (p<0.001) in patients of type 2 diabetes with diabetic vascular complications compared with the group of type 2 patients without diabetic vascular complications and the control group (72.1±5.2, 59.5±4.7, and 36.9±4.4 ng/ ml, respectively).
|
| |
1- السكري من النمط الثاني Type II diabetes السكري هو مجموعة من الأمراض الاستقلابية تتصف بفرط سكر الدم hyperglycemia، الناجم عن خلل في: إفراز الأنسولين، أو تأثير الأنسولين أو كليهما. يترافق فرط سكر الدم المزمن في الداء السكري بضرر طويل الأمد مصحوباً بخلل وظيفي وفشل في العديد من الأعضاء؛ وخاصة العين، الكليتين، الأعصاب والأوعية الدموية. يشكل المصابون بالسكري من النمط الثاني حوالي 90-95% من مجموع المصابين بالسكري، ويكون معظم مرضى هذا النمط بدينين، حيث تسبب البدانة بحد ذاتها درجة معينة من المقاومة للأنسولين. يتظاهر عند هؤلاء المرضى ارتفاع في غلوكوز الدم، يتصاحب مع مستويات أنسولين مرتفعة أو طبيعية وتكون وظيفة الخلايا البنكرياسية طبيعية. أي أنَ هنالك خللاً في وظيفة الأنسولين المفرز، حيث يكون غير كافٍ لتعويض مقاومة تأثير الأنسولين(1).
تعد إمراضية السكري معقدة، وهي تتضمن التفاعل ما بين عوامل جينية وبيئية. حيث يبدي المريض بالسكري من النمط الثاني ثلاثة شذوذات أساسية:
• مقاومة لفعالية الأنسولين في النسج المحيطية، خاصة في العضلات والنسج الشحمية وكذلك الكبد؛
• خلل في إفراز الأنسولين، خاصة كاستجابة لتنبيه الغلوكوز؛
• زيادة إنتاج الغلوكوز عن طريق الكبد(2).
2- مضاعفات السكري
تقسم المضاعفات إلى نمطين:
1. داء الأوعية الدقيقة Microvascular disease: مجموعة اعتلالات خاصة بالسكري تحدث على مستوى الأوعية الدقيقة في شـبكية العين، والكبيبات الكلوية والأعصاب المحيطية.
2. داء الأوعية الكبيرةMacrovasculer Disease: يتصف بالتصلب العصيدي الذي يتفاقم بوجود السكري، ويصيب الشرايين التي تغذي القلب، والدماغ، والأطراف السفلية.
يُعد السكري المسبب الأساسي للعمى الذي يحصل ما بين 20-74عاماً من العمر. يشكل المرضى السكريين الفئة الأسرع تطويراً للاعتلال الكلوي وزرع الأعضاء. إن أكثر من 60% من المرضى السكريين يصابون بالاعتلال العصبي، والذي يتضمن الاعتلال العصبي المتعدد المتناظر الذي يصيب الأعصاب البعيدة، واعتلال الأعصاب الوحيد، بالإضافة إلى مجموعة من الاعتلالات العصبية التلقائية والتي تسبب فشلاً في الوظيفة الانتصابية، وسلساً بولياً، وخزلاً هضمياً، وإسهالاً انتيابياً. يزداد اختطار الأمراض الوعائية القلبية من مرتين إلى ست مرات عند المرضى السكريين، ويتوقع أن تكون فترة بقائهم على قيد الحياة أقصر بحوالي 7-10 سنوات من المرضى غير المصابين بالسكري(3).
3- الهيالورونان Hyaluronan
يعرف الهيالورونان بأنه غلوكوز أمين غليكاني موجود بوفرة في المطرس خارج الخلوي، له وظائف حيوية مميزة. تكمن أهميته في تحقيق التجمع الصحيح للأنسجة البينية، وقدرته على التأثير في سلوك الخلية، من خلال ارتباطه بمجموعة من مستقبلات تنبيغ الإشارة، أهمها CD44(4). وتكمن أهميته الحيوية في ما يلي:
يلعب دوراً أساسياً في هجرة الخلايا خلال التخلق morphogenesis، التنشـؤ الوعائي
angiogenesis، انتشار الأورام والنقائل؛
يتدخل في احتباس، وتنظيم والتقام endocytosis المواد خارج الخلوية الغنية بالهيالورونان؛
يتواسط التصاق وتكوّر اللمفاويات؛
يسهم في تنسيق إشارات المطرس الخلوي والتوازن ما بين سبل موت وعيوشية الخلايا.
وذلك من خلال الدور الهام لمعقد هيالورونان-CD44 في تنبيغ الإشارة(5).
4- الهيالورونان وعلاقته بالسكري
ذكرت العديد من الدراسات العالمية أن هنالك زيادة في إنتاج الهيالورونان في الجسم تحت تأثير فرط سكر الدم، ولا بد هنا من ذكر دراسة Jones وزملاؤه عام 2001، والتي تعد أول دراسة لزيادة تخليق الهيالورونان من قبل خلايا الأنبوب الكلوي القريب المُحرّض بإضافة 25 mmol/L من D-Glucose، أو تحت تأثير السيتوكين طليعة الالتهاب IL-1Β. حيث فسّرت هذه الدراسة أن زيادة التخليق سببها تفعيل انتساخ إنزيم الهيالورونان سينثاز من النمط الثاني HAS2، نتيجة تفعيل انتساخ عامل الانتساخ النووي nuclear factor κB NF-κB(6).
يطرأ تبدل على استقلاب العديد من مكونات العضوية تحت تأثير فرط سكر الدم والمقاومة للأنسولين، بما فيها مكونات المطرس خارج الخلوي. ففي دراسة Chajara وزملاؤه عام 2000 على نموذج Zuker rat، وهو يشابه النموذج الاستقلابي للبشر المصابين بالسكري غير المعتمد على الأنسولين، جرى إحداث إصابة وعائية بوساطة القثطرة. وقد أظهرت الدراسة زيادة في إنتاج الهيالورونان في بطانة الشريان والطبقة الوسطى، وذلك في مكان إحداث الإصابة الوعائية. يمكن أن يفسر هذا الزيادة الملاحظة في فعالية الخلايا العضلية الملساء في منطقة الإصابة عند هذه المجموعة من الجرذان(7).
يبدأ تشكل العصيدة الشريانية في بطانة الشريان، حيث تتصف بتسمك هذه الطبقة بسبب تراكم الخلايا وعناصر المطرس خارج الخلوي وجزيئات الهيولى مثل البروتينات الشحمية الحاملة للكوليستيرول. يتواجد الهيالورونان في كل طبقات العصيدة، وغالباً ما يتركز حيث تتواجد العناصر الرابطة له مثل الفاريسكان.
إن إحداث إصابة بوساطة قثطرة البالون عند حيوانات موضوعة على حمية غنية بالدهن يسبب تطور آفة التصلب العصيدي، حيث تتطور هذه الآفة في بطانة الشريان وتتصف بزيادة في عدد الخلايا العضلية الملساء والبالعات، بالإضافة إلى تراكم عناصر المطرس خارج الخلوي. يزداد الهيالورونان في مناطق تطور الآفة حيث تكون هنالك هجرة وتكاثر للخلايا العضلية الملساء. تقترح هذه الدراسات أن الهيالورونان يؤثر في تكاثر وهجرة الخلايا العضلية الملساء خلال تطور التصلب العصيدي(8). وبالتالي فإن الهدف من هذه الدراسة هو تعيين مستويات الهيالورونان المصلية لدى المصابين بالسكري من النمط الثاني وتقييم دوره في التنبؤ عن حدوث المضاعفات الوعائية لدى المرضى السكريين.
|
| المواد والطرق Materials and Methods |
شملت دراستنا 87 فرداً موزعين إلى المجموعات التالية:
- المجموعة الشاهدة: شملت أفراداً أسوياء ظاهرياً (11 ذكراً، و 12 أنثى)، لا يعانون من السكري ولا يتناولون أية أدوية، متوسط أعمارهم X±SD: 50.8 ±12 عاماً.
- المجموعات المرضية:
المجموعة A: شملت مرضى سكريين من النمط الثاني (16 ذكراً، و 16 أنثى)، لم يشخص لديهم أي نمط من مضاعفات السكري، يتناولون أحد خافضات السكر الفموية منذ عام على الأقل، متوسط أعمارهم X±SD: 51.7±9.9 عاماً.
المجموعة B: شملت مرضى سكريين من النمط الثاني (13 ذكراً، و 12 أنثى)، حيث جرى تشخيص نمط واحد على الأقل من مضاعفات الداء السكري لديهم: اعتلال بصري، أو كلوي، أو عصبي أو داء الأوعية التاجية، متوسط أعمارهم X±SD: 50.3±8.7 عاماً، ويمثل الشكل 1 مخططاً لتوزع مجموعات الدراسة.
جمعت العينات في الفترة مابين 1/5 / 2009 و51/12/2009 من مراجعي المراكز الطبية التالية:
• مستشفى المواساة الجامعي، شعبتي الأمراض الداخلية وأمراض الغدد الصم؛
• المركز الطبي التخصصي للسكري التابع لوزارة الصحة.
وقد جرى انتقاء المرضى من المصابين بالسكري من النمط الثاني، والمعالجين لفترة لا تقل عن عام بأحد خافضات السكر الفموية و/ أو الأنسولين، ولقد جرى استثناء المرضى الذين لديهم قصة إدمان على الكحول، أو المصابين بأمراض كبدية. كما جرى استثناء مرضى الديال الكلوي، ومرضى التهاب المفاصل الروماتويدي، والتهاب المفصل العظمي osteo arthritis OA، والتصلب الجهازي المتقدّم PSS، والذئبة الحمامية الجهازية SLE. وقد اعتمد على بيانات مراقبة المرضى ضمن المستشفى لأخذ معلومات حول وجود أحد مضاعفات السكري ونمط هذه المضاعفات. كما جرى الاعتماد على اختبار مقايسة البيلة الألبومينية الزهيدة microalbuminurea لتأكيد وجود الاعتلال الكلوي.
أخذت عينات الدم على الريق بعد صيام ليلة كاملة في الفترة ما بين الساعة الثامنة والعاشرة صباحاً، وقد جرى الاعتيان على النحو التالي:
عينات المصل: بزل 5 مل دم وريدي على أنبوب جاف، وجرى التنبيذ مباشرة (3000 دورة في الدقيقة مدة 5 دقائق)، ووزع المصل الناتج ضمن ثلاثة أنابيب إيبندورف. حُفظت العينات عند الدرجة - 20°م إلى حين إجراء المقايسات. استخدمت القسيمة الأولى لكل عينة لمقايسة الهيالورونان والقسيمة الثانية لمقايسة الغلوكوز والقسيمة الثالثة بقيت قسيمة احتياطية.
عينات الدم الكامل: وُضع1.5 مل دم وريدي في أنبوب يحوي مضاد تخثر (EDTA)، وقد جرى استخدامها لمقايسة الهيموغلوبين السكري مباشرة بعد جمع العينة.
عينات البول: جُمع 2 مل من البول الصباحي من أجل الكشف عن البيلة الألبومينية الزهيدة. وجرى جمع عينات المجموعة الشاهدة من متطوعين أصحاء لا يراجعون أي مركز طبي. ولقد أجريت المقايسات التالية:
مقايسة مستويات الهيالورونان المصلية بطريقة الامتزاز المناعي المرتبط بالإنزيم ELISA. أجريت المقايسة باستخدام عتيدة hyaluronan ELISA kit المصنعة من قبل شركة Corgenix الأمريكية. ويعتمد مبدأ العمل بهذه العتيدة على استخدام البروتين الرابط للهيالورونان (HABP) Hyaluronan Binding Protein الموجود طبيعياً والمستخلص من الغضروف البقري ليقوم بالتقاط جزيئات الهيالورونان نوعياً، كما تستخدم العتيدة البروتين الرابط للهيالورونان والمقترن بالإنزيم لتحري ومقايسة الهيالورونان المُلتقط من عينات المصل أو البلازما البشرية.
مقايسة الهيموغلوبين السكري
جرت المقايسة باستخدام عتيدة لشركة Biosystem الاسبانية، وتعتمد على استخدام الأعمدة مبادلة الشوارد.
مقايسة الغلوكوز
استخدمنا الطريقة الإنزيمية (Glucose GOD /PAP) لمقايسة مستويات الغلوكوز في المصل.
مقايسة البيلة الألبومينية الزهيدة microalbuminurea
جرت المقايسة باستخدام عتيدة لشركة Biosystem الاسبانية، وتعتمد على مبدأ المعايرة بمقياس العكر turbidimetry.
|
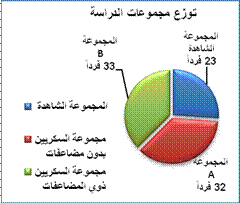
الشكل 1: توزع مجموعات الدراسة. |
| النتائج Results |
جرت مقايسة مستويات الهيالورونان لدى أفراد المجموعة الشاهدة (23 فرداً سوياً)، فوجد أنها تتراوح بين28.7 -45.1 نغ/ مل (36.9±4.36 نغ/ مل(. كما جرت مقايسة الهيالورونان لدى مرضى السكري من النمط الثاني، والذين جرى تقسيمهم إلى مجموعتين على أساس تشخيص وجود المضاعفات الوعائية للسكري. ويبين الجدول 1 النتائج.
جرت مقايسة مستويات الهيموغلوبين السكري لدى مجموعات الدراسة. ولقد تراوحت القيم لدى مجموعة مرضى السكري بدون مضاعفات (المجموعة A) بين 5.5- 7.7% (X±SD: 6.5%± 0.63%)، ولدى مجموعة السكريين ذوي المضاعفات (المجموعة B) 5.5-8.3% (X±SD: 7.1%± 0.7%)، ولدى المجموعة الشـاهدة بين 4.2-5.8% (المتوسـط الحسابي
4.9%±0.55%)، ويبين الشكل 2 ما سبق.
جرت مقايسة مستويات الغلوكوز لدى مجموعات الدراسة بالطريقة الإنزيمية (GlucoseGOD/PAP). تراوحت القيم لدى مجموعة مرضى السكري بدون مضاعفات وعائية (المجموعة A) بين 130- 187 ملغ/ دل (X±SD: 159.8±15.18 ملغ/ دل)، ولدى مجموعة المرضى السكريين ذوي المضاعفات (المجموعة B) 156.2-198.1 ملغ/ دل (X±SD:180.4 ±12.5 ملغ/ دل) ولدى المجموعة الشاهدة بين 83-110 ملغ/ دل (X±SD:101.1 ±7.1 ملغ/ دل)، ويبين الشكل 3 ما سبق.
عند دراسة العلاقة بين مستويات الهيالورونان المصلية ومستويات غلوكوز المصل، وجد لدينا علاقة ارتباط إيجابية (R=0.45) ومعتد بها (P<0.001)، ويبين الشكل 4 ما سبق.
عند دراسة علاقة الارتباط بين مستويات الهيالورونان المصلية ومستويات الهيموغلوبين السكري، وجدت علاقة ارتباط إيجابية (R=0.33) يعتد بها إحصائياً (p=0.007)K ويبين الشكل 5 ما سبق.
|
الجدول1: قيم الهيالورونان لدى مرضى السكري من النمط الثاني في المجموعات السريرية المدروسة ومقارنتها مع المجموعة الشاهدة.
المجموعة المدروسة |
عدد العينات |
متوسط قيم الهيالورونان (نغ/مل) |
الانحراف المعياري |
قيمة p مقابل الشاهد |
المجموعة الشاهدة |
23 |
36.9 |
4.36 |
|
المجموعة A |
32 |
59.5 |
4.7 |
<0.001 |
المجموعة B |
33 |
72.1 |
5.2 |
<0.001 |
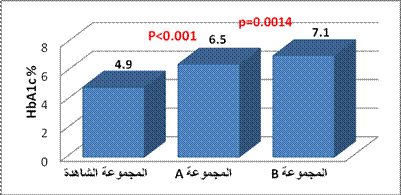
الشكل 2 : قيم الهيموغلوبين السكري لدى مجموعات الدراسة.
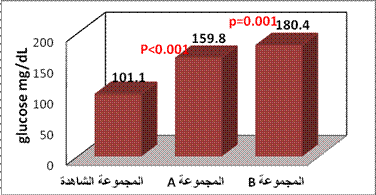
الشكل 3 : قيم الغلوكوز الصيامي لدى مجموعات الدراسة.
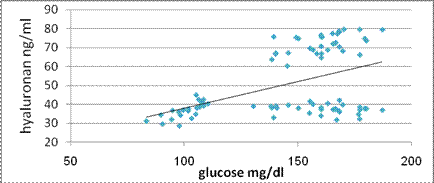
الشكل 4 : علاقة الارتباط ما بين قيم الهيالورونان المصلية المقاسة وقيم الغلوكوز الصيامي
لدى أفراد الدراسة.
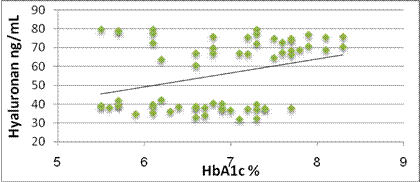
الشكل 5 : علاقة الارتباط ما بين مستويات الهيالورونان المقاسة وقيم الهيموغلوبين السكري
لدى أفراد الدراسة.
|
| المناقشة Discussion |
لقد أظهرت دراستنا ارتفاعاً يعتد به إحصائياً في متوسط القيم المصلية للهيالورونان لدى م
ضى السكري من النمط الثاني (X±SD: 59.5±4.7 نغ/ مل)، حيث بتطبيق اختبار T -Student لوحظ وجود فارق يعتد به إحصائياً ما بين مجموعة مرضى السكري من النمط الثاني دون أي نمط من المضاعفات للسكري (المجموعة A)، والمجموعة الشاهدة (P<0.001).
ولقد وجدت العديد من الدراسات العالمية أن فرط سكر الدم يزيد من إنتاج الهيالورونان في العديد من الأنسجة وجرى تفسير ذلك من خلال ما يلي:
لقد أثبتت دراسة Stuart Jones وزملاؤه عام 2001 أن فرط الغلوكوز يفعل عامل الانتساخ nuclear factor- κB (NF-κB) في خلايا الأنبوب الكلوي القريب. وقد أثبت Stuart Jones وزملاؤه أن تفعيل NF-?B يقود إلى تفعيل انتساخ إنزيم اصطناع الهيالورونان HAS2 مؤدياً بذلك إلى زيادة اصطناعه(6).
كما توافقت دراستنا مع الدراستين العالميتين التاليتين:
دراسة Yerneni وزملاؤه عام 1999(9)، ودراسة L. Rugheimer وزملاؤه عام 2008 (10).
كما وجدنا من خلال دراستنا فارقاً يعتد به ما بين متوسط قيم الهيالورونان لمجموعة مرضى السكري والذين يعانون من أحد المضاعفات الوعائية للسكري، بالمقارنة مع المجموعة الشاهدة ومجموعة مرضى السكري بدون مضاعفات وعائية (72.1±5.2، 59.5±4.7، 36.9±4.4 نغ/ مل، على الترتيب).
ربطت العديد من الدراسات العالمية ما بين زيادة تخليق الهيالورونان وتطور مضاعفات الأوعية الدقيقة(11)، وأيضاً مضاعفات الأوعية الكبيرة والتصلب العصيدي(12). ويمكن تفسير ما سبق من خلال الدور المعروف للهيالورونان في تنظيم تكاثر وهجرة الخلايا العضلية الملساء الوعائية(8)، وفي تجنيد الكريات البيضاء وجذبها إلى موضع الآفة(13)، وهذا يشير إلى دور الهيالورونان في الآلية الإمراضية للاعتلالات الوعائية، توافقت بذلك دراستنا مع الدراسات التالية:
دراسة Aled Lewis وزملاؤه عام 2008 والتي وجدت أن الهيالورونان هو مشعر للتليف بين الخلايا interstitial fibrosis وموجود عند كل مرضى الدراسة ذوي الاعتلال الكلوي السكري(11).
دراسة Song Chai وزملاؤه عام 2007 والتي تشير نتائجها إلى أن التراكم المنتشر للهيالورونان يسرّع تطور التصلب العصيدي(12).
ارتبطت كل من مستويات الغلوكوز الصيامية والهيموغلوبين السكري إيجابياً مع مستويات الهيالورونان المصلية، وهذا يتفق مع فكرة أن زيادة تخليق الهيالورونان يرتبط مع ترقي فرط سكر الدم، وحالة عدم ضبط السكري، حيث ترتبط مستوياته إيجابياً مع متثابتات ضبط السكري القصيرة والطويلة الأمد(14).
وبالتالي من المحتمل أن تعكس مستويات الهيالورونان المصلية حالة الضعف العام لجدران الأوعية الدموية الذي يسببه فرط سكر الدم بسبب الضبط غير الملائم لغلوكوز الدم عند المرضى السكريين، وتوافقت دراستنا مع دراسة shinichiro MINE عام 2006(14).
|
| الاستنتاج Conclusion |
|
ترتفع تراكيز الهيالورونان عند المرضى السكريين من النمط الثاني، ويعكس هذا عدم انضباط غلوكوز الدم. يقترح ما سبق إمكانية استخدام مستويات الهيالورونان المصلية كواصم للتنبؤ بالاعتلال الوعائي السكري.
|
| المراجع References |
1-American Diabetes Association: Diagnosis and Classification of Diabetes Mellitus,.
Diabetes Care, 33: 62-69, 2010.
2-John B. Buse, Kenneth S. Polonsky and Charles F. Burant
Type 2 Diabetes Mellitus, Kronenberg: Williams Textbook of Endocrinology.
11th ed, Henry M. Kronenberg, Shlomo Melmed, Kenneth S. Polonsky, P. Reed Larsen.
Publisher: Saunders: 1329-1358, 2007.
3-Michael Brownlee, Lloyd P. Aiello, Mark E. Cooper, Aeron I. Vinik, Richard W. Nestro and Andrew J. M. Boulton.
Complications of Diabetes Millitus, Kronenberg: Williams Textbook of Endocrinology, 11th ed, Henry M. Kronenberg, Shlomo Melmed, Kenneth S. Polonsky, P. Reed Larsen.
Publisher: Saunders:1417-1478, 2007.
4-Tammi M.I; Day A.J. and Turley E.A.
Hyaluronan and homeostasis: a balancing act.
J. Biol. Chem; 277, 4581-4584, 2002.
5-Warren Knudson and Cheryl B. Knudson
The Hyaluronan Receptor ,CD44. Un update. Science of Hyaluronan Today, 2004.
6-Jones S; Jones S. and Phillips AO.
Regulation of renal proximal tubular epithelial cell hyaluronan generation: implications for diabetic nephropathy.
Kidney International, 59: 1739-1749, 2001.
7-Chajara A; Raoudi M; Delpech B; Leroy M; Basuyau JP. and Levesque H.
Increased hyaluronan and hyaluronidase production and hyaluronan degradation in injured aorta of insulin-resistant rats.
Arterioscler Thromb Vasc Biol; 20: 1480-1487, 2000.
8-Thomas N. Wight
Hyaluronan in Atherosclerosis and Restenosis.
Science of HyaluronanToday,1999.
9-Yerneni KKV; Bai W; Khan BV. et al.
Hyperglycaemia induced activation of nuclear transcription factor kB in vascular smooth muscle cells.
Diabetes; 48: 855-864, 1999
10-Rügheimer L; Carlsson C; Johnsson C. and Hansell P.
Renal hyaluronan content during experimental uncontrolled diabetes in rats.
Journal of physiology and pharmacology, 59(1): 115-128, 2008.
11-Aled Lewis, Robert Steadman, Paul Manley, Kathrine Craig, Carol Motte, Vincent Hascall and Aled O. Phillips
Diabetic nephropathy, inflammation, hyaluronan and interstitial fibrosis.
Histol Histopathol, 23: 731-739, 2008.
12-S. Chai ; Q. Chai ; C. C. Danielsen ; P. Hjorth ; J. R. Nyengaard ; T. Ledet ; Y. Yamaguchi ; L. M. Rasmussen ; and Lise Wogensen Bach, Overexpression of Hyaluronan in the Tunica Media Promotes the Development of Atherosclerosis, Circulation Research.;96:583-591, 2005.
13-Brian Ruffell, Pauline Johnson. The Regulation and Function of Hyaluronan binding CD44 in the Immune System. Science of Hyaluronan Today, 2009.
14-Shinichiro Mine,Yosuke Okada, Chie Kawahara,Takahiro Tabata,Yoshiya Tanaka. Serum hyaluronan concentration as a marker of angiopathy in patients with diabetes mellitus.endocrine journal 53, 761-766, 2006.
|
| المجلد 5 ,
العدد 10
, المحرم 1432 - كانون ثاني (يناير) 2011 |
|
|
|
