| المجلد 5 ,
العدد 9
, شوال 1431 - تشرين أول (أكتوبر) 2010 |
| |
| المضادات الحيوية والمقاومة الجرثومية |
| Antibiotics and Bacterial Resistance |
| د. عبد السلام العمر |
| Abdul Salam AL-Omar |
|
| الملخص Abstract |
يعد اكتشاف البنسلين والستربتوميسين في مطلع القرن الماضي، عاملاً حاسماً في تراجع اختطارات الأمراض المعدية، وإنقاذ أعداد كبيرة من المصابين من موت محقق بفعل جراثيم إيجابية وسلبية الغرام. تتالت الاكتشافات وبلغت أوجها بين عامي 1930-1970، حيث يتوافر حالياً في الأسواق ما يزيد على 100 مضاد حيوي من أجيال مختلفة. تجلت فعالية المضادات الحيوية المدهشة في تخفيض معدل وفيات الخدج، وحديثي الولادة، انتان السحايا، ومرضى العناية المشددة، مرضى عوز المناعة بفعل الأورام الخبيثة وغيرها، وإطالة عمر البقيا (البقاء على قيد الحياة). تشتمل الانتانات الجرثومية الأكثر مساهمة في امراضية الانسان، والتي بدورها تحمل في طياتها ظهور المقاومة وانتشارها، على: الاسهالات، انتانات الجهاز التنفسي، التهاب السحايا، الأمراض المنتقلة بالجنس، الانتانات المكتسبة في المستشفيات، أما العوامل الممرضة والمسؤولة بصورة رئيسية عن ظهور المقاومة وانتقالها فتتضمن: المكورات الرئوية المقاومة للبنسلين PRSP، المكورات المعوية المقاومة للفانكوميسين VRE، المكورات العنقودية المقاومة للأوكساسيلين/ للمثيسيلين MRSA، السلمونيله متعددة المقاومة MDR-SA، والمتفطرات السلية متعددة المقاومة MDR-TB (1).
ينتج عن ظهور المقاومة وانتشارها بين الجراثيم عواقب جمة، تبدأ بعدم استجابة المريض للعلاج بمضادات حيوية تنتمي إلى الخط الأول، اطالة المرض وتعريض صحة المريض لاختطار حقيقي قد ينتهي بالوفاة. تشكل زيادة المرضى الحاملين لجرثومة مقاومة للمضادات الحيوية خطراً على صحة الناس في المجتمع أو المرضى والعاملين في المستشفيات وتجعلهم مصدراً مستمراً لنقل هذه الجراثيم وازدياد عدد الحملة لها (1). ان مقاومة الجراثيم للمضادات الحيوية ظاهرة حيوية طبيعية، تزداد أو تتناقص تبعاً للممارسات الخاطئة أو الصحيحة لكلٍ من الطبيب المعالج بما في ذلك الطبيب البيطري والمريض والصيدلي والمستشفيات وشركات ووكلاء الأدوية ووزارة الصحة والجهات الاعلامية.
تعتبر مشكلة ظهور المقاومة وانتشارها بين الجراثيم على المستوى الوطني أو الأممي عالمية بامتياز ويجب أن تضع كل ادارة وطنية خطة متكاملة للتعامل مع هذا الخطر باعتباره يهدد صحة المواطنين ويستنزف ثروتها الوطنية، لازدياد التكاليف المالية. يستدعي ذلك تقيد العاملين في قطاع الصحة /خاصة المجموعات المتعاملة مباشرة مع المضادات الحيوية والانتانات/ بالتعليمات والإرشادات الموضوعة من قبل الجهات المختصة وتشكيل وحدات أو مجموعات صغيرة من الخبراء، لمتابعة ذلك على صعيد المجتمع وعلى صعيد المستشفيات، وهنا لابد من الاستفادة من البرامج التي وضعتها منظمة الصحة العالمية في هذا الخصوص، كونها تهتم بهذه المشكلة الصحية على صعيد العالم. وهنا يشار إلى الكتيب الصادر عن منظمة الصحة العالمية والالتزام بمضمونه (2).
|
| المقاومة |
هناك طرق وآليات متعددة لاكتساب المقاومة من قبل الجراثيم:
* ان لطريقة استخدام المضادات الحيوية دوراً هاماً وحيوياً في انتقاء الجراثيم لمقاومة المضادات الحيوية المستخدمة، كما يحصل للزمرة الجرثومية المستوطنة في المستشفيات، والتي تنتقل إلى مرضى المستشفيات، لعصيات السلمونيلا التي تستوطن المرارة أو للمكورات العنقودية المقاومة للميثيسيلين في أنوف الحملة.
* الأشواط العلاجية غير كافية بما في ذلك توريد غير كاف للمضادات الحيوية، وعدم التزام وتقيد المريض بمواعيد تناول الدواء وكميته، يمكن أن يتسبب في ازدياد المقاومة، كما هو الحال لدى المتفطرات السلية. يشير مصطلح MDR-TB إلى مقاومة العصيات السلية لكل من: ايزونيازيد وريفامبين، ويشير مصطلح XDR-TB إلى مقاومة واسعة للمتفطرات السلية إلى: ايزونيازيد وريفامبين وأي مركب من الفلوروكينولون وعلى الأقل واحداً من العقاقير التي تعطى حقناً مثل كابريومايسين، كاناميسين أو أميكاسين (3).
العقاقير المضادة للجراثيم
تقسم بحسب تأثيرها على الجراثيم إلى ثلاث مجموعات:
* قاتلة للجراثيم: زمرة البيتالاكتام بما في ذلك البنسيلينات، السيفالوسبورينات، كاربابنم ومونوباكتام، زمرة غليكوبيبتايد ممثلة بفانكوميسين وتايكوبلانين، فلوروكينولونات، أمينوغليكوزيدات، ميترونيدازول، ريفامبين وهي فعالة في معالجة التهاب شغاف القلب، التهاب السحايا، تجرثم الدم، الأمراض الجهازية ومرضى عوز المناعة.....
* مثبطة لنمو الجراثيم: أهمها ماكروليدات (ايريثرومايسين..)، تتراسكلين ولينكوزأميدات (لينكومايسين وكليندامايسين).
* مثبطة عموماً وقاتلة خصوصاً للجراثيم: يمثلها كلورامفينيكول فهو مثبط لنمو الجراثيم عموماً، لكنه قاتل لكلٍ من المستدميات النزلية HI، والمكورات الرئوية SP والنيسريات السحائية NM.
بنية الخلية الجرثومية وآليات تأثير المضادات الحيوية
تقسم الجراثيم شكلاً ولوناً إلى مجموعتين كبيرتين: ايجابيات الغرام وتتلون بالأزرق البنفسجي، وسلبيات الغرام وتتلون بالأحمر. في كل مجموعة توجد جراثيم لها أهمية كبيرة من الناحية الطبية فمن ايجابيات الغرام لدينا المكورات العنقودية SA، العقديات الحالة للدم والمكورات الامعائية. ومن سلبيات الغرام لدينا عائلة العصيات الامعائية، الزوائف الزنجارية PA، المستدميات النزلية HI، والنيسريات البنية NG، والسحائية NM.
يظهر الشكل 1 بنية عامة لخلية جرثومية بمكوناتها المختلفة من المحفظة، فالجدار الخلوي فالغشاء السيتوبلازمي، وأخيراً السيتوبلازما وما تحتويه من المادة الوراثية DNA والريبوزومات (4).
أما الشكل 2 فيظهر بنية الجدار الخلوي للجراثيم سلبية وايجابية الغرام، حيث تبدو سماكة طبقة ببتيدوغليكان المكون الرئيسي للجدار الخلوي لدى ايجابيات الغرام ((20-80 nm، أما لدى سلبيات الغرام فتكون طبقة ببتيدوغليكان أقل سماكة (5-10 nm) وتغطى من الخارج بالغشاء الخارجي المؤلف بصورة أساسية من عديد سكاريد شحمي وبروتين شحمي (4).
أما الشكل 3 فيظهر مراحل تكوين البروتينات بداية من قراءة DNA من قبل RNA-polymers، وقطع سلسلة DNA المضاعفة لنسخها، ومن ثم عودة التحامها من قبل إنزيم DNA-gyrase. يقوم كل من mRNA، tRNA، 30s Subunit، 50s Subunit، Amino Acids و 70s Ribosoms بالدور المنوط به في تصنيع البروتينات الأساسية للخلية الجرثومية (5).
يتركز تأثير مجموعة بيتالاكتام متمثلة بالبنسيلينات (Ps)، السيفالوسبورينات (CEPHs)، كاربابنم (CARB) ومونوباكتام (MONOB) إضافة إلى فانكوميسين (VA) وتايكوبلانين (TEI) على طبقة ببتيدوغليكان، وتحول دون تركيبها بشكل كامل مما يؤدي إلى خلخلة الجدار الخلوي وتهدم الخلية الجرثومية.
أما المضادات الحيوية التي تؤثر على تكوين الحمض الريبي النووي منقوص الأكسجين (دنا=DNA) مباشرة، فتشمل مركبات السلفا وثريميثوبريم حيث تتشابه مع حمض باراأمينوبنزويك (PABA)، وتمنع تشكيل حمض الفوليك Folic Acid الضروري لبناء DNA.
|
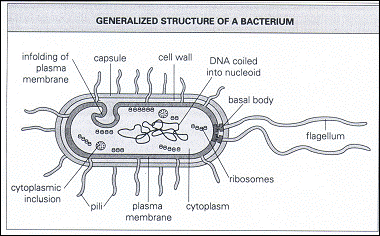
الشكل 1 : بنية عامة لخلية جرثومية بمكوناتها المختلفة.
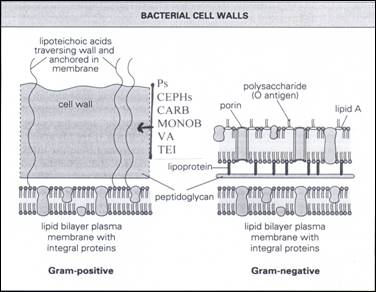
الشكل 2 : يظهر بنية الجدار الخلوي للجراثيم سلبية وايجابية الغرام.
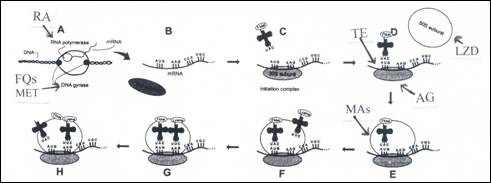
الشكل 3 : مراحل تكوين البروتينات.
|
المجموعة الأهم هي التي تحصر تصنيع وتركيب البروتينات الضرورية للجراثيم وهي:
* ريفامبين (RA) يرتبط مع RNA-polymers ويمنع نسخ mRNA اعتباراً من DNA.
* فلوروكينولونات (FQs) تستهدف DNA-Gyrase وتمنع نهايتي DNA المقطوع من عودة الالتحام.
* ميترونيدازول (MTN) يؤثر على DNA-Gyrase وعلى وظيفة الغشاء السيتوبلازمي.
* أمينوغليكوزيدات (AG) ترتبط بشكل غير عكوس (قاتلة للجراثيم) بتحت الوحدة 30s وتمنع التحامها مع تحت الوحدة 50s لتشكيل الريبوزوم.
* تتراسيكلين (TE) يرتبط بشكل عكوس مع تحت الوحدة 30s مشوهة اياها وبذلك تعيق الراموزات الموجودة على tRNA من الاتحاد مع الراموزات المقابلة لها والموجودة على mRNA.
* أوكسازوليدينونات (لينيزوليد LZD) مضاد حيوي جديد يرتبط مع تحت الوحدة 50s ويحول دون التحامها مع معقد البدء.
* ماكروليدات MAs (كليندامايسينCC ، لينكوميسين) ترتبط بتحت الوحدة 50s بشكل عكوس وتمنع تشكل الروابط الببتيدية ما بين الأحماض الأمينية وتمنع الريبوزم 70s من التحرك أسفل mRNA (5).
|
مشاكل استخدام المضادات الحيوية بشكل غير مناسب
* تشمل الحصيلة الرئيسية لاستخدام المضادات الحيوية بشكل غير مناسب على تفاعلات جانبية للعقار غير مرغوب بها، ظهور جراثيم مقاومة ومتعددة المقاومة، خمج ثانوي اضافي وزيادة التكاليف المادية المصروفة، فمثلاً سجلت 43% من حالات استخدام غير مناسب للمضادات في تركيا و 37.4 % في هولندا.
* تستخدم المضادات الحيوية للوقاية من الانتانات ما قبل وأثناء العمل الجراحي. يعتبر الاستخدام المطول (أكثر من 36 ساعة)، وغير الملائم، واحداً من سلبيات وصف المضادات الحيوية، وقد بلغت نسبة سوء الاستخدام 15% في أمريكا، 72% في السويد، 58.3% في فرنسا، 47.7- 98% في تركيا، مع ملاحظة ازدياد معدل انتانات عداوي المستشفيات.
* تعدت الوقاية باستخدام المضادات الحيوية قبل وأثناء العمل الجراحي يوم واحد في 80% و 3 أيام في 68.2% بدراسة أجريت على 3004 مريض في تايوان.
* لم تضف الوقاية المطولة أثناء العمل الجراحي أية فائدة في منع عدوى المستشفيات في الموضع الذي تمت فيه الجراحة.
* تُعد المعالجة المبنية على نتائج الزرع الجرثومي أو الهادفة عاملاً هاماً في خفض معدل الاستخدام غير المناسب للمضادات الحيوية.
* هذه المشكلة موجودة أيضاً في المجتمع، للأسف بصورة خاصة في المجتمعات النامية حيث لا يوجد رقابة على صرف المضادات الحيوية واسعة الطيف، والتي يجب أن تصرف من قبل أطباء فقط، وليس من قبل الصيدلي.
* في دراسات أجريت في مراكز متعددة وجد أن 51.9% من المرضى، لم يأخذوا كافة الجرع المخصصة لهم، وبلغت هذه النسبة 13.5% في هولندا، و 90% في الصين، ووجد أن عدداً كبيراً من المرضى الذين يتم وصف المضادات الحيوية لهم بوصفة لم ينهوا العلاج كاملاً مقارنة مع المرضى الذين يسجل لهم عدد محدد من الجرعات العلاجية.
* يرتبط سوء استخدام المضاد الحيوي أحياناً وإلى درجة معينة بعقيدة وقناعة شخصية للطبيب، مع الرغبة في التمرد على المعطيات العلمية الحديثة والتمسك بمعلوماته القديمة.
* آخراً لكن ليس أخيراً فان الجهود التشجيعية النشطة لشركات الأدوية، يمكن أن تؤثر سلباً، وتزيد في سوء استخدام المضاد الحيوي، وقد وجد كل من كورال وسمين أن الهدايا التشجيعية من قبل الشركات، تؤثر في انتقاء الدواء بحوالي 43% من قبل الأطباء (6، 7، 10، 15).
كيف يمكننا انقاص مقاومة الجراثيم للمضادات الحيوية
* بداية وحقيقة تقال أن التخلص نهائياً من المقاومة غير ممكن، وتطوير الجراثيم للمقاومة أمر محتم.
* لاحتواء أو / و لإنقاص المقاومة الحاصلة حالياً لا بد من اللجوء إلى الاستخدام الأمثل للمضادات الحيوية المتوفرة، ولاستخدام خيارات المعالجة البديلة، مثل تقوية المناعة من خلال التمنيع الفاعل (التلقيح)، بإعطاء لقاح المكورات العنقودية، النيسريات السحائية، المكورات الرئوية..، تحسين التغذية (8).
* منع ظهور وانتشار المقاومة لاحقاً باستخدام تقنيات حديثة للتعرف وللتشخيص الباكر للجراثيم المقاومة، وتخفيض فوعة الجرثوم المعزول.
* تثقيف الطاقم الصحي والمرضى، ووضع سياسات لاستخدام المضادات الحيوية، والعمل بموجب الأنظمة النافذة، وتقييد استخدام المضادات الحيوية واسعة الطيف.
انتقاء المقاومة لمجموعة بيتالاكتام من قبل المكورات الرئوية:
تشتمل عوامل الخطورة المترافقة بتواتر أكبر لعزل ذراري مكورات رئوية مقاومة للبنسيلينات على:
* اسـتمرار استخدام المضادات الحيوية بالشكل
الحالـي، بما في ذلك، عـدم كفاية الجرعـات
المأخوذة، أو إطالة فترة العلاج أكثر من اللازم، مرحلة المراهقة، التواجد في دور رعاية الطفولة، والإقامة في مناطق ذات معدل وقوع عال.
* تُعد المضادات الحيوية من زمرة بيتالاكتام، الماكروليدات والسلفا- ثريميثوبريم، قادرة على احداث انتقائية لذرارٍ مقاومة.
* أدى انقاص استخدام المضادات الحيوية إلى انخفاض معدلات حملة مكورات رئوية مقاومة للبنسيلينات، ففي ايسلندا بلغ هذا المعدل 19.8% عام 1992 وتناقص إلى 13% عام 1997 ويعود ذلك إلى أنه تم تطبيق برنامج في ايسلندا أدى إلى انخفاض قدره 10% في استخدام المضادات الحيوية.
* ينبغي على الأطباء أن يكونوا قادرين على تمييز الحالات التي لا يكون فيها اعطاء المضاد الحيوي ضرورياً، وإذا ما كانت الحالة ضرورية لوصف مضاد حيوي، فالقاعدة الهامة هي أن يختار الطبيب العقار الأكثر ملائمة والأضيق طيفاً، الأقل تكلفة وسمية، الجرعة الأمثل والفترة العلاجية الأنسب (6، 14).
دعم وتقوية البرامج المنظمة لاستخدام وترصد المضادات الحيوية:
* ان التطور متعدد الاتجاهات، والأنظمة واعتماد الممارسة والمعالجة المبنية على البرهان، وإتباع الارشادات الناظمة لعلم الجراثيم، ومراقبة انتشارها في مكان العمل، وتوفير نماذج تحسسها ومقاومتها، كلها يمكن أن تحسن من استخدام المضادات الحيوية بما في ذلك الوقاية قبل وأثناء العمل الجراحي.
* من المهم أيضاً التوصل لمعرفة الجرعة العلاجية المثلى اعتماداً على خصائص المريض الشخصية، العمرية والجنسية، العامل الأكثر احتمالاً، أو المسبب للانتان، موضع العدوى والخصائص الحركية والديناميكية للمضاد الحيوي.
* ان وضع خطة منهجية للتحول بالمضاد الحيوي من اعطائه بالطريق الداخلى إلى الطريق الفموي مع توافر حيوي ممتاز في موضع الخمج إذا ما سمحت حالة المريض يمكن أن ينقص من مدة اقامة المريض في المستشفى وبالتالي تخفيض التكلفة.
* الالمام التام بالمعالجة المشاركة، ايجابياتها وقلة سلبياتها.
* وجوب توفر تخويل مسبق وتقيد رسمي باستخدام المضادات الحيوية. في عام 2003 قامت الحكومة التركية بوضع خطط لاستخدام المضادات الحيوية :
- مضادات حيوية تخضع لقيود أثناء صرفها وتشمل:
Teicoplanin (TP), Vancomycin (VA), Imipenem (IPM), Meropenem (MEP), Piperacillin (PIP/Tazobactam).
- مضادات حيوية تصرف من قبل الأطباء الاختصاصين دون الحاجة لموافقة أخصائي الأمراض المعدية في المستشفيات ولمدة 3 أيام فقط وهي:
Ceftriaxone (CRO), Cefotaxime (CTX), Ceftazidime (CAZ), Cefixime (CFM), Ciprofloxacin (CIP), Amikacin (AN), Netilmicin (NET), Levofloxacin (LVX), Cefoperazone (CFP).
- ما تبقى من المضادات الحيوية يمكن وصفها من قبل كافة الأطباء.
خلال 8 أشهر انخفضت كلفة المضادات الحيوية بحدود 19.6% (ما يعادل 540303 دولار) مع ملاحظة أن معدل الوفيات بقي دون تغيير في حين انخفض معدل عداوى المستشفيات بصورة ملحوظة. انخفضت مقاومة Kleb. Pneumonia للأميكاسين من 30 إلى 19%، للسيفوروكسيم من 55 إلى 37% وللأوغمنتين من 59 إلى 46% أما ذراري Kleb. Pneumonia والتي كانت ايجابية لإنزيم ESBL+ انخفضت من 49 إلى 35%. انخفض معدل المقاومة لدى MRSA المعزولة من 70 إلى 55%.
* وجوب توفر تخويل مسبق يمكن أن يتسبب أحيانا في جدال قوي مابين الأطباء المعالجين والجهات الضابطة لصرف المضادات الحيوية (6، 7، 9، 11، 12).
كيف نحسن معالجة المتفطرات السلية متعددة وواسعة المقاومة للمضادات الحيوية MDR and XDR-Tb
- توفر مختبر متخصص يؤمن نماذج التحسس والمقاومة للمضادات الحيوية.
- توفر مختبر متخصص يوفر زرع ذراري المتفطرات السلية وعزلها وتحدد هويتها.
- اللجوء إلى خطط عمل تعتمد الملاحظة والمتابعة المباشرة لتناول العلاج.
- تسهيل الوصول إلى عقاقير الصف الثاني في حالة احتياجها.
- تطوير تقنيات قادرة على كشف نماذج مقاومة المتفطرات دون الحاجة إلى زرعها (3).
فوائد وعوائق كامنة وراء استخدام مضادات الجراثيم ضيقة الطيف
يعتمد في تحديد المضادات الحيوية ضيقة الطيف على طيف (عدد) الجراثيم التي تمتلك فعالية ضدها وتشمل البنسيلين، غليكوببتيدات، ماكروليدات، نتروفورانتوئين، ميترونيدازول، ازتريونام، ناليدكسيك أسيد وفوسفومايسين وتستخدم في حالات انتانات الجهاز البولي غير المختلطة، التهاب البلعوم والجيوب.
فوائد الاستخدام:
- المحافظة على الزمرة الجرثومية الطبيعية والتي يمكن أن تساعد في تخفيض مخاطر الخمج المختلط.
- هذه العقاقير لا تستهدف محددات مقاومة متعددة وهي بذلك أقل احتمالاً في حصول انتقاء مقاومة لها من قبل الجراثيم.
عوائق الاستخدام:
- الحاجة إلى وضع تشخيص دقيق وسريع للحالة المرضية.
- غير قادرة على معالجة الانتانات المسببة بأكثر من جرثومة واحدة بنفس الوقت.
- هناك صعوبة في تسويقها (6-7).
فوائد وعوائق كامنة وراء استخدام مضادات الجراثيم واسعة الطيف:
تشتمل المضادات الحيوية واسعة الطيف على كاربابنم، سيفالوسبورينات، بيتالاكتام (مركبات مشاركة مثبطة لإنزيم بيتالاكتاماز)، فلوروكينولونات وأمينوغليكوزيدات.
فوائد الاستخدام:
- الأمان (شعور بالطمأنينة) الذي يتولد لدى الطبيب المعالج من استخدام هذه المضادات في التعامل مع الآليات الانتانية المسببة بعامل ممرض غير معروف (مجهول).
- دور وأهمية هذه المضادات في تدبر الانتانات المسببة بجرثومتين أو أكثر.
عوائق الاستخدام:
- مقدرة كبيرة كامنة في قتل الزمرة الجرثومية الطبيعية مقارنة مع مضادات حيوية ضيقة الطيف ومايترتب عن ذلك أحيانا من حالات مرضية مثل التهاب القولون المترافق بالأغشية الكاذبة بفعل المطثيات الصعبة Clostridium difficile.
- مقدرة كامنة في انتقاء محددات مقاومة لدى جراثيم متعددة.
- مقدرة كامنة في انتقاء وتهيئة الظروف لنمو مفرط لجراثيم معينة مثل مكورات معوية مقاومة للفانكومايسين (VRE).
- المعالجة بهذه المضادات يمكن أن يخلق شعورا خاطئاً بالأمان.
يعلق الدكتور Moellering قائلا:
Narrow is nice, If you can live with it, and broad is bad, except when you need it.
(المضادات الحيوية ضيقة الطيف جيدة اذا استطاع الطبيب أن يسخرها للحالة التي يعالجها، المضادات الحيوية واسعة الطيف سيئة، ماعدا الحالات التي يتوجب فيها استخدامها للعلاج) (6 و 7).
استخدامات المضادات الحيوية واسعة الطيف:
- بصورة تجريبية قبل أن يتم تحديد هوية العوامل المسببة للالتهاب أو الانتان وبصورة أساسية في الحالات المهددة للحياة مثل التهاب السحايا، ذات الرئة، التهاب شغاف القلب ومثيلاتها.
- لمعالجة الجراثيم المقاومة، التي لا تستجيب لمضادات أخرى مثل مضادات ضيقة الطيف.
- في الأخماج المختلطة المسببة بجراثيم متعددة اما أحادية أو بمعالجة مشاركة (7).
|
وبائيات مقاومة الجراثيم للمضادات الحيوية في المجتمع
تُعد المقاومة مشكلة عالمية تزايد ظهورها في المجتمع. فعلى صعيد الزمرة الجرثومية الطبيعية أدى الاستخدام الواسع وسوء الاستعمال للفانكوميسين في معالجة التهاب القولون المشكل لغشاء كاذب pseudomembranous colitis المسبب من قبل المطثية Clostridium difficile إلى انتقاء وظهور ذرارٍ من مكورات معوية Enterococcus faecium مقاومة للفانكومايسين VRE وفي هذا الصدد يعد ميترونيدازول عقار الصف الأول في معالجة هذه الحالة المرضية (6). ان عزل ذراري مكورات عنقودية مقاومة للفانكومايسين VRSA من انوف حملة في المجتمع يدل على الاستخدام الواسع للفانكومايسين في المجتمع وعدم خضوعه لقواعد ناظمة لصرف المضادات الحيوية. لوحظ زيادة في معدلات عزل ذراري كلٍ من المكورات الرئوية (14)، والنيسريات البنية المقاومة للبنسيلين في المجتمع كما وسجل ازدياد أعداد عصيات الايشريكية القولونية والكلبسيلا الرئوية التي تنتج إنزيم بيتالاكتام واسع الطيف ESBL+ بحيث تمتد مقاومتها لأفراد الجيل كاملة كما هو الحال مع مضادات الجيل الثالث للسيفالوسبورينات. فعلى سبيل المثال في السعودية بلغ عدد الحملة للجراثيم الايجابية لإنزيم ESBL+ في البراز 26.1% (272 مريض مقيم في المستشفى)، 15.4% (162 مريض خارج المستشفى) و 13.1% (426 شخص سليم). في اسبانيا بلغ عدد الحملة للامعائيات الايجابية لإنزيم ESBL+ 6.6%، أما في تركيا فبلغ عدد الايشريكية القولونية ايجابية ESBL+ المعزولة من الجهاز البولي 7.9% وفي الهند 34.4% (6).
بمقارنة نماذج تحسس ومقاومة عصيات العائلة الامعائية (الجدول 1 و 2) المعزولة من عينات مرضية مرسلة للمختبر من عيادات المجتمع خلال 29 شهراً من الفترة الواقعة بين 2007- 2009 مأخوذة من سجلات المختبر (الجدول 1) وبين 2002-2004 (13) (الجدول 2) كما هو وارد في الجداول أسفل.
مقارنة نموذج التحسس (S%)، التحسس المتوسط (I%) والمقاومة (R%) المئوية للمضادات الحيوية بالنسبة لعائلة العصيات الامعائية المعزولة من عينات بول مرضى العيادات الخارجية من المجتمع مابين 2007-2009 (الجدول 1) و 2002-2004 (الجدول 2) (13).
تبين أنه حصل تغير في النسب المئوية لنماذج التحسس والمقاومة حيث لوحظ زيادة في معدلات مقاومة عصيات العائلة الامعائية لبعض المضادات الحيوية (الجدول 3). سجل تراجع في مقاومة هذه العصيات للبعض الآخر (الجدول 4) وبقيت المقاومة كما هي لدى CTX.
أظهرت مقارنة نماذج تحسس ومقاومة المكورات العنقودية الذهبية (الجدول 5 و 6) المعزولة من عينات مرضية مرسلة للمختبر من عيادات المجتمع خلال 29 شهراً من الفترة الواقعة بين 2007-2009 مأخوذة من سجلات المختبر (الجدول 5) وبين 2002-2004 (13) (الجدول 6) كما هو وارد في الجداول أسفل مقارنة نموذج التحسس (S%)، التحسس المتوسط (I%) والمقاومة (R%) المئوية للمضادات الحيوية بالنسبة للمكورات العنقودية الذهبية المعزولة من عينات مرضى العيادات الخارجية في المجتمع ما بين 2007-2009 (الجدول 5) و 2002-2004 (الجدول 6) (13).
أن التغيـر الحاصل في نسب التحسس والمقاومة
للمضادات تجاه المكورات العنقودية الذهبية سجل زيادة في المقاومة لبعضها (الجدول 7)، بينما لوحظ تراجع في مقاومة هذة المكورات للبعض الأخر (الجدول 8).
تشير هذه الجداول إلى التغير المستمر في نماذج المقاومة والتحسس للمضادات الحيوية تبعا لآليات وصف وصرف هذه العقاقير المتبعة والتي تختلف من منطقة لأخرى، حيث تزيد مقاومة جرثوم ما للمضاد الحيوي كلما سهل صرفه من الصيدلية وزاد وصفه من الطبيب في معالجة الحالة الانتانية خاصة في المعالجة التجريبية Empiric Therapy. في هذا الخصوص يشار مرة أخرى وليست أخيرة إلى أهمية ضبط وتنظيم وصف وصرف المضادات الحيوية في المجتمع. ان توافر نماذج التحسس والمقاومة الدورية على مكاتب الأطباء المعالجين سوف يحد من سوء استخدامها، وينقص من ظهور وانتشار المقاومة ويوفر على المريض الكثير من الوقت والجهد والمال للوصول إلى الشفاء.
حددت منظمة الصحة العالمية أن 4% من حالات المتفطرات السلية المكتشفة حديثاً تكون متوسطة المقاومة للمضادات ففي استونيا بلغت هذه النسبة 2.5%، ألمانيا 5.7%، ايطاليا 2.8% وتركيا 7.9%. تتواجد المتفطرات السلية واسعة المقاومة في البلدان حيث تتواجد المتفطرات السلية متعددة المقاومة (3 و 6).
|
الجدول 1
2007-2009 |
AM |
AML |
AMC |
CF |
CTX |
CRO |
NA |
NOR |
OFL |
CIP |
GM |
AK |
SXT |
F/M |
CXM |
S% |
8 |
18 |
22 |
15 |
74 |
82 |
60 |
77 |
68 |
50 |
73 |
91 |
53 |
75 |
62 |
R% |
85 |
72 |
69 |
48 |
21 |
14 |
30 |
21 |
27 |
50 |
17 |
7 |
44 |
14 |
25 |
I% |
7 |
10 |
9 |
37 |
5 |
4 |
10 |
2 |
5 |
0 |
10 |
2 |
3 |
11 |
13 |
الجدول 2
2002-2004 |
AM |
AML |
AMC |
CF |
CEC |
CTX |
CRO |
NA |
NOR |
OFL |
CIP |
GM |
AK |
SXT |
F/M |
S% |
22 |
28 |
36 |
16 |
67 |
74 |
71 |
66 |
78 |
59 |
69 |
81 |
85 |
37 |
72 |
R% |
68 |
66 |
39 |
50 |
16 |
24 |
21 |
27 |
20 |
33 |
25 |
19 |
15 |
55 |
17 |
I% |
10 |
6 |
25 |
34 |
17 |
2 |
8 |
7 |
2 |
8 |
6 |
0 |
0 |
8 |
11 |
الجدول 3
|
AM |
AML |
AMC |
CF |
GM |
NA |
NOR |
CIP |
ازدياد المقاومة % |
13 |
9 |
15 |
1 |
7 |
5 |
1 |
18 |
الجدول 4
|
F/M |
AN |
CRO |
OFL |
SXT |
تراجع المقاومة % |
2 |
6 |
11 |
9 |
16 |
الجدول 5
2007-2009 |
AM |
AML |
AMC |
CF |
GM |
SXT |
F/M |
CIP |
DOX |
CC |
OX |
FEP |
VA |
S% |
8 |
26 |
66 |
77 |
56 |
50 |
96 |
70 |
87 |
83 |
80 |
81 |
100 |
R% |
88 |
64 |
29 |
19 |
39 |
47 |
0 |
27 |
4 |
9 |
20 |
14 |
0 |
I% |
4 |
10 |
5 |
4 |
5 |
3 |
4 |
3 |
9 |
8 |
0 |
5 |
0 |
الجدول 6
2002-2004 |
AM |
AML |
AMC |
CF |
GM |
SXT |
F/M |
CIP |
DOX |
S% |
7 |
28 |
69 |
97 |
44 |
48 |
100 |
31 |
61 |
R% |
93 |
44 |
31 |
0 |
50 |
52 |
0 |
62 |
22 |
I% |
0 |
28 |
0 |
3 |
6 |
0 |
0 |
7 |
17 |
الجدول 7
|
AM |
CF |
AML |
AMC |
F/M |
ازدياد المقاومة % |
1 |
20 |
2 |
1 |
4 |
الجدول 8
|
SXT |
DOX |
GM |
تراجع المقاومة % |
2 |
26 |
12 |
|
وبائيات مقاومة الجراثيم للمضادات في المستشفيات:
تختلف المقاومة للمضادات من جناح إلى جناح ضمن المستشفى ومن مستشفى لآخر. لاتميز الجراثيم المقاومة بين الحدود وبين الدول فهي عالمية. تسبب مقاومة الجراثيم للمضادات مشاكل جمة، كما هو الحال مع الزوائف الزنجارية، أسينيتوباكتر باومانئي، الكلبسيلا، المكورات العنقودية المقاومة للميثيسيلين و المكورات المعوية المقاومة للفانكوميسين حيث تبدي حساسية لصنف واحد أو صنفين من المضادات الحيوية وربما تصبح ذرارٍ ذات مقاومة واسعة وربما شاملة (6 و 7). ان الانتانات المسببة بذرارٍ ذات مقاومة واسعة تكون عادة مرتبطة باطالة المكوث في المستشفى، بزيادة التكلفة، وبمعدل وفيات عال حيث تشكل المقاومة تحد كبير للطاقم الطبي. تلعب لجنة مراقبة العدوى في المستشفيات Infection control committee دوراً هاماً في تخفيض معدل عدوى المستشفيات Nosocomial Infection Rate حيث تراقب بصورة يومية الانتانات بالتعاون مع المختبر الجرثومي وتعمل على عزل المرضى المصابين بانتان ذي خطورة عالية وخاصة المخموجين بجرثوم متعدد المقاومة. ان لفعالية لجنة عدوى المستشفيات ولاخصائي عدوى المستشفيات من خلال تشاوره مع الطبيب المعالج دورا هاما في ترصد وجعل معدلات الجراثيم متعددة المقاومة المعزولة تحت السيطرة وفي المجال المسموح به.
ماذا عن المستقبل/ نظرة إلى خمس سنوات قادمة/:
يوجد حالياً عوامل مضادة للجراثيم واعدة مثل لينزوليد، تيغسيكلين، كوينوبرستين/ دالفوبرستين، أوريتافانسين، دالبافانسين، دابتومايسين، سيفتابيبرول لمعالجة الجراثيم ايجابية الغرام متعددة المقاومة للمضادات. يجري العودة إلى مضادات حيوية قديمة مثل فوسفومايسين وكولستين واجراء البحوث والتجارب لتقدير امكانية استخدامها في معالجة الجراثيم سلبية الغرام متعددة للمقاومة.
ان الأبحاث المرتبطة بملتهمات الجراثيم واستخداماتها تتزايد طرداً ومعدلات انتشار الجراثيم واسعة المقاومة للمضادات الحيوية وقد وجد أن المعالجة بها أقل تكلفة من استخدام فانكوميسين وتايكوبلانين ولينزوليد في معالجة الانتانات المسببة بالعنقوديات المقاومة. يقوم المتخصصون بتحليل ودراسة الطاقة والقوة المحرضة للمضادات الحيوية في توليد مقاومة لها وامكانية جعل المضادات الحيوية مصدر أساسي لكربون الجراثيم. سيزداد أعداد الدول التي ستطبق سياسات تحديد وتقييد استخدام المضادات الحيوية لما في ذلك من تأثير في تخفيض معدلات الجراثيم المقاومة المعزولة، كما ستزيد الاجراءات المرتبطة بمراقبة وترصد عدوى المستشفيات واستخدام اللقاحات لدى البالغين (6، 7، 11).
|
| References المراجع |
1-World Health Organisation
Antimicrobial Resistance, Fact sheet No 194, revised January 2002.
2-Consultations and Workshop, Critically Important Antimicrobials for Human Medicine. Report of the second WHO Expert Meeting.
Copenhagen, 29-31 May 2007, World Health Organisation.
3-Matteeli A. et al.
Multidrug-resistant and Extensively drug-resistant M. tuberculosis. Epidemiology and Control.
Expert Rev. Anti. Infet. Ther. 5(5), 857-871, 2007.
4-Medical Micrbiology, Mims. Playfair. Roitt. Wakelin. Williams, M Mosby 1993.
5-MedStudy, Internal Medicine, Core Curriculum 2007-2008, Book 1, Infectious Disease.
6-Economics of Antibiotic Resistance.
Expert Rev. Anti. Infect. Ther, 2008.
7-WWW.medscape.com/Economics of Antimicrobial Resistance
8-Coast J. and Smith RD.
Antimicrobial Resistance. Cost and Containment.
Expert Rev. Anti. Infect. Ther. 1, 241-251, 2003.
9-Usluer G. et al.
Turkish antibiotic Utilization Study Group.
Ann. Clin. Microbial. Antimicrob. 4, 16, 2005.
10-Mandell Douglas and Bennett S.
Principles and Practice of infectious Disease.
Churchil Livingstone, PA. USA, 3177-3191, 2000.
11-Garau J.
Impact of Antibiotic Restrictions.
Clin. Microbiol. Infet. 12 (Suppl. 5) 16-24, 2006.
12-Petrak MR. et al.
The Value of an Infectious Disease
Specialist.
Clin. Infect. Dis. 36, 1013-1017, 2003.
13-Al-Omar Abdul Salam
Bacterial Culture Results and Susceptibility Test of Uropathogens isolated from Outpatients referred from Clinics in Community. 3(7), 2005.
14-Joseph P. Lynch, George G. Zhanel
Streptococcus Pneumoniae: Does Antimicrobial Resistance Matter? From Seminars in Respiratory and Critical Care Medicine. WWW.medscape.com/Abstracts and Introduction 1-37, 2009.
15-Predictros of Broad-Spectrum Antibiotic Prescribing for Acute Respiratory Tract Infections in Adult Primary Care.
JAMA. 289(6): 719-725, 2003.
|
الملحق 1: فحص تحسس الجراثيم المعزولة للصادات الحيوية
يجب الاشارة الى أنه ومنذ ما قبل عام 1990 تم الغاء نظام الزوائد (+، ++، +++) في تقدير حساسية، متوسط الحساسية ومقاومة الجراثيم للصادات الحيوية، لذا يجب التوقف عن تسجيلها على التقرير الصادر عن المختبر. يجب الالتزام بالنظام الجديد القديم المعترف عليه من قبل ادارة العقاقير والأغذية الأمريكية (FD)، منظمة الصحة العالمية (WHO) واللجنة الوطنية للمقاييس المخبرية السريرية (NCCLS). هذا النظام يستخدم الأقراص المشربة بتركيز محدد من صاد حيوي لإجراء فحص التحسس نصف الكمي بالاستعانة بطريقة انتثار الصاد الحيوي من القرص على سطح الأغار. هذه الطريقة وهذا النظام شائعي الاستخدام عالمياً للجراثيم التي تنمو بسرعة وبعض الجراثيم العطوبة وتشمل عصيات العائلة الإمعائية، جنس المكورات العنقودية، الزوائف الزنجارية، أسينيتوباكتر، المكورات المعوية وضمات الهيضة. أما الطرق المعدلة باستخدام أوساط زرعية انتقائية مثل Chocolate Agar, Modified Thayer-Martin, Mueller Hinton Blood Agar وغيرها فيستفاد منها في فحوص تحسس المكورات الرئوية، النيسيريات البنية والمستدميات النزلية وغيرها.
بحسب هذا النظام وبعد قراءة دقيقة بالمسطرة الى أقرب ميليمتر لقطر تحسس الجرثوم تصنف نتلئج التحسس الى ثلاث: جرثوم مقاوم (R) اذا كان قطر التحسس أصغر من الحد الأدنى المسموح به جرثوم متحسس (S) اذا كان قطر التحسس أكبر من الحد الأعلى المبين جرثوم متوسط الحساسية (I) اذا كان قطر التحسس يقع مابين الحد الأدنى والأعلى وذلك بحسب التعليمات المرفقة بالنشرة أو في الجدول الملحق (> أكثر أو يساوي، < أقل أو يساوي).
Adapted from BD BBLtm Sensi-Disc Antimicrobial Susceptibility Test Discs (2004/9)
|
|
| |
| |
| |
| المجلد 5 ,
العدد 9
, شوال 1431 - تشرين أول (أكتوبر) 2010 |
|
|
|
