| الملخص Abstract |
طُوِّرت طريقة جديدة لمقايسة النِسْتاتين ضمن أشكاله الجرعية الصيدلانية باستخدام جهاز HPLC ذي الطور العكوس RP- HPLC، مع طور متحرك مؤلف من 70% ميثانول + 20% ماء + 10% ثنائي ميثيل فورماميد. كان معدل الجريان 1 مل/ د وفق نظام الاستشراب المتساير. كما استخدم مكشاف الأشعة فوق البنفسجية بموجة طولها 305نانومتراً.
طُوِّرت أيضاً طريقة لمقايسة النِسْتاتين ضمن أشكاله الجرعية الصيدلانية باستخدام جهاز الطيف الضوئي بالأشعة فوق البنفسجية في موجة طولها 305 نم، حيث استخلصت العينات بواسطة الميثانول وحمض الأسيتيك الثلجي.
لقد جرى التحقق من مصدوقية الطريقتين وكانت متثابتات تَوثيقُ المَصْدوقِيَّة جميعها ضمن المجال المقبول.
|
A new method has been developed to assay Nystatin in its pharmaceutical dosage forms by using RP- HPLC, with a mobile phase consisting of 70% methanol + 20% water + 10% dimythelformamide. The flow rate was 1 ml/min according to the isocratic chromatography. A UV detector has been used with a wavelength 305 nm.
Also other method was developed to assay Nystatin in its pharmaceutical dosage forms by using UV- spectrophotometer at wavelength 305 nm, where the samples had been extracted by methanol and glacial acetic acid.
The assay methods have been validated, and all validation parameters were within the acceptance range.
|
| المقدمة Introduction |
لقد ازدادت الإصابات الفطرية عند البشر بشكل ملحوظ في السنوات الأخيرة من ناحية نسب الحدوث وشدة الإصابة، ويعود ذلك بشكل رئيسي إلى التطور في الجراحة، وعلاجات السرطان، والعناية المشددة المترافقة مع زيادة استعمال المضادات الحيوية واسعة الطيف، بالإضافة إلى متلازمة نقص المناعة المكتسب AIDS، مما أدى إلى ازدياد أعداد المرضى المؤهبين للإصابة بالعداوى الفطرية (1).
يعد النِسْتاتين من الأدوية الهامة لعلاج الأمراض الفطرية لامتلاكه فعالية جيدة مضادة للفطريات، ولتأثيراته الجانبية القليلة نسبياً، مقارنة مع الأدوية الأخرى المضادة للفطريات (1). لذا فقد كان الهدف من الدراسة العملية في هذا البحث:
تطوير طرق جديدة لمقايسة النِسْتاتين تتميز بالدقة والحساسية والنوعية وسهولة التطبيق وذات تكلفة اقتصادية مقبولة، بحيث تكون قادرة على فصل النِسْتاتين عن السواغات ونواتج التخرب وذلك لاستخدامها في مقايسته كمادة أولية وفي أشكاله الصيدلانية.
الطرق المطورة لمقايسة النِسْتاتين
* الطريقة الأولى: المقايسة باستخدام الاسْتِشْرابُ السَّائِلُ الرَّفيعُ الإِنْجَازHPLC ، وذلك بالاستفادة من طريقة Kay R. Bagon (2) لمقايسة النِسْتاتين في أشكاله الصيدلانية وطريقة Juan M. Llabot, Daniel A. Allemandi, Ruben H. Manzo, Marcela R. Longhi) (3) لمقايسته في اللعاب.
* الطريقة الثانية: المقايسة باستخدام مقياس الطيف الضوئي بالأشعة فوق البنفسجية UV spectrophotometer.
|
| المواد Materials |
• ماء خاص بجهاز HPLC + ميثانول + ثنائي ميثيل الفورماميد DMF + حمض الأسيتيك الثلجي من شركة Panreac.
• معياري النِسْتاتين من شركة VUAB Pharma a.s قوته potency تساوي 6479 وحدة دولية/ ملغ.
|
| الأجهزة Equipments |
• حمام للأمواج فوق الصوتية Ultrasonic T310 (Germany).
• مقياس باهاء pH meter.
• مراشح HPLC: قياس 0.45 µmلشركة Sartorius Stedium Biotech.
• عمود HPLC:inertcil ODS - 3 (5 µm ، 4.6 × 250 mm)، من شركة Japan) ،GL Science Inc).
• جهاز HPLC: KNAUER مزود بمكشاف UV/VIS (Germany).
• جهاز الطيف الضوئي بالأشعة فوق البنفسجية JASCO V- 530 UV/VIS.
|
| تحضير العينات: |
تحضير عينات الأقراص لطريقة المقايسة باستخدام HPLC:
جرى تحضير عينتين لأقراص النِسْتاتين (كل قرص تحوي 500000 وحدة دولية من النِسْتاتين) وفق ما يلي:
* وزنت عشرة أقراص نِسْتاتين، وسحقت ومزجت جيداً، ثم أخذ من المسحوق25 ملغ، واستخلص بواسطة 100 مل من مزيج مؤلف من 70% ميثانول + 20% ماء +10 % DMF.
* وضِع المحلول في حمام للأمواج فوق الصوتية لمدة نصف ساعة حتى الذوبان التام للنِسْتاتين، ثم جرى تنبيذه بعد ذلك.
تحضير عينات المعلق لطريقة المقايسة باستخدام HPLC:
حُضرت عينتان لمعلق النِسْتاتين (كل 1 مل يحوي 100000 وحدة دولية من النِسْتاتين) وفق ما يلي:
* جرى خض عبوة معلق النِسْتاتين بشكل جيد، وأخذت منه كمية موزونة بدقة تحوي العدد نفسه من الوحدات الدولية الموجودة في 25 ملغ من مسحوق الأقراص، واستخلصت بواسطة 100 مل من مزيج الاستخلاص السابق، ثم وضع المحلول في حمام للأمواج فوق الصوتية لمدة نصف ساعة، جرى تنبيذه بعد ذلك.
تحضير محلول النِسْتاتين المعياري لطريقة المقايسة باستخدام HPLC:
* جرى تحضير محلول معياري يحوي العدد نفسه من الوحدات الدولية المفترض وجودها في محلول العينات وهو 36127.465 وحدة دولية، حيث جرى استخلاص 5.575 ملغ من المعياري بواسطة 100 مل من مزيج الاستخلاص السابق، ثم وضع المحلول في حمام للأمواج فوق الصوتية لمدة نصف ساعة، جرى تنبيذه بعد ذلك.
تحضير الطور المتحرك لطريقة المقايسة باستخدام HPLC:
حُضِّر مزيج مؤلف من 70% الميثانول + 20% الماء +10 % DMF، فكانت pH = 6.1.
تحضير محلول النِسْتاتين المعياري لطريقة المقايسة باستخدام UV:
* أذيب 30.868 ملغ من معياري النِسْتاتين (تحوي الكمية 200000 وحدة دولية) في مزيج من 5 مل حمض الأسيتيك الثلجي و 50 مل من الميثانول باستخدام جهاز الأمواج فوق الصوتية لمدة ربع ساعة حتى الذوبان التام للنِسْتاتين، ثم أكمل الحجم إلى 100 مل، بعد ذلك مدد 1 مل من المحلول السابق حتى 100 مل بالميثانول (4).
تحضير عينات المعلق لطريقة المقايسة باستخدام UV:
حُضِّرت ثلاث عينات لمعلق النِسْتاتين (كل 1
مل يحوي 100000 وحدة دولية ) وفق ما يلي:
* حُضّرت عبوة معلق النِسْتاتين، وأخذت منها كمية موزونة بدقة تحوي 200000 وحدة دولية، ثم أضيف إليها 10 مل ماء مقطر ومُزجت بشكل جيد، ثم جرى تنبيذ المحلول مدة نصف ساعة بسرعة 2500 دورة/ د.
* بعد ذلك فصل الماء بالإبانة وأُذيب الراسب بالمزيج المستخدم كما في مراحل تحضير محلول المعياري.
تحضير عينات الأقراص لطريقة المقايسة باستخدام UV:
حُضّرت ثلاث عينات لأقراص النِسْتاتين (كل قرص يحوي 500000 وحدة دولية) وفق ما يلي:
* سحقت عشرة أقراص للنِسْتاتين، ومزجت جيداً، وأخذت كمية موزونة بدقة من المسحوق تحوي 200000 وحدة دولية، ثم أضيف لها 10 مل ماء مقطر ومُزجت بشكل جيد، ثم جرى تنبيذ المحلول مدة نصف ساعة بسرعة 2500 دورة/ د. بعد ذلك فصل الماء بالإبانة وأذيب الراسب بالمزيج المستخدم كما في مراحل تحضير محلول المعياري.
|
| طريقة المقايسة بالاستشراب السائل رفيع الإنجاز HPLC: |
الشروط الاستشرابية
The chromatographic conditions
* ضُبِط معدل التدفق عند 1 مل/ د، و بموجة مكشاف طولها 305 نانومتراً.
* رُشحت كمية من محلول عينة المعياري عبر مرشـحة HPLC 0.45 مكرومتر، وحقن 2
مكرولتر منها داخل العمود المستخدم.
* جرى تكرار العملية السابقة مع محاليل عينات الأقراص والمعلقات.
|
| النتائج Results |
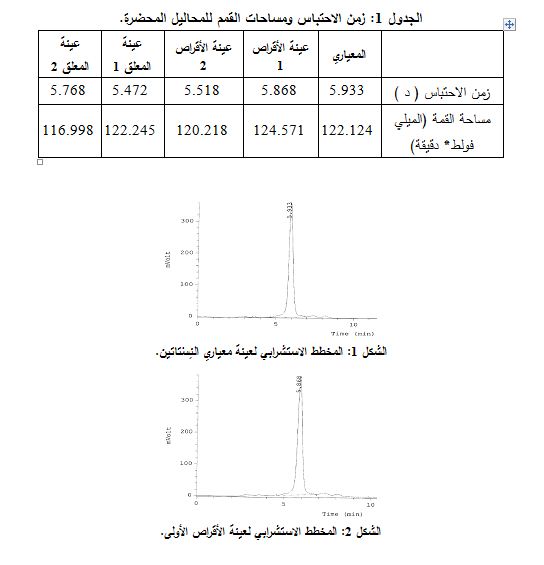
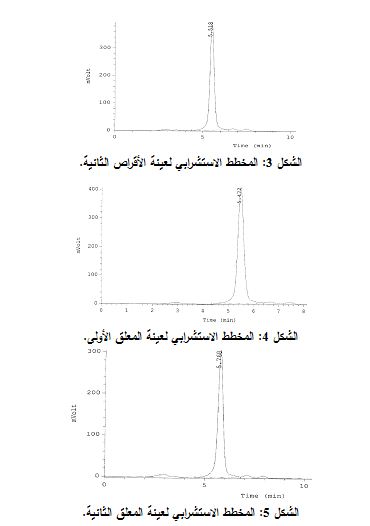
يبين الجدول 1 خصائص المحاليل المحضرة بالطرق المذكورة سابقاً. كما توضح الأشكال 1-5 المخططات الاستشرابية للعينات المدروسة. كما جرى حساب تراكيز النِسْتاتين على الشكل التالي:
تركيز النِسْتاتين الفعلي في القرص مقدراً بالنسبة المئوية = (مساحة قمة عينة القرص/ مساحة قمة المعياري) × (قوة المعياري × وزنه) × (متوسط وزن القرص / وزن العينة المأخوذة من مسحوق القرص) × (100/ 500000).
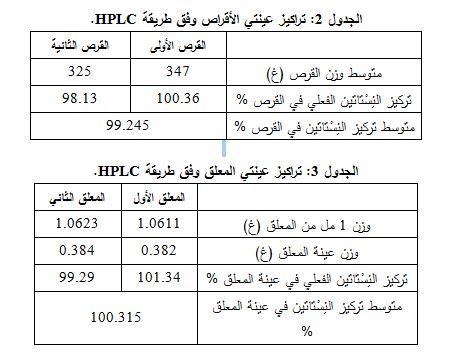
* تركيز النِسْتاتين في 1 مل من المعلق مقدراً بالنسبة المئوية = (مساحة قمة عينة المعلق/ مساحة قمة عينة المعياري) × (قوة المعياري × وزنه) × (وزن 1 مل من المعلق/ وزن العينة المأخوذة من المعلق) × (100/ 100000). ويبين الجدولان 2 و3 تراكيز النِسْتاتين في العينات المدروسة وفق طريقة HPLC
|
|
| التحقق من مصدوقية الطريقة Method validation |
* ملاءمة النظام System Suitability:
حُقنت خمس عينات متتالية من محلول النِسْتاتين المعياري لإجراء اختبار ملاءمة النظام، فكانت أهم المعايير الدستورية للمخطط الاستشرابي موافقة لمتطلبات مركز أبحاث وتقييم الدواء (CDER) Center of Drug Evaluation and Research (5-8).
* المضبوطية Accuracy:
حُقنت خمس عينات متتالية من محلول معياري النِسْتاتين فكان الانحراف المعياري النسبي RSD أقل من 2%. حُضرت ثلاث عينات للنِسْتاتين تركيزها 80% من تركيز المعياري، وثلاث عينات تركيزها 100%، وثلاث عينات تركيزها 120%، ثم حُقنت العينات المحضرة وحسبت الاستعادة recovery، ثم حسب المتوسط فكان 99.13% (5-8).
* الدقة Precision:
- قابلية إعادة النتائج أو التناتج Reproducibility: (عند إجراء التناتج لا داعي لإجراء الدقة الوسطى): حُقنت خمس عينات متتالية من محلول معياري النِسْتاتين فكان RSD أقل من 2%. ثم أخذت ست عينات من محلول للنِسْتاتين بتركيز 100 % من المعياري، وحقنت بشروط المقايسة ذاتها، ثم كررنا الحقن في مختبر آخر فكان RSD = 0.93.
- التكرارية repeatability أو قابلية تكرار النتائج: حُقنت خمس عينات متتالية من محلول معياري النِسْتاتين فكان RSD أقل من 2%، ثم حُقنت تسع عينات من محلول للنِسْتاتين بتركيز 100% من المعياري، فكانت قيمة RSD=0.20 (5-8).
* النوعية Specificity:
حُضّر محلول يحتوي على السواغات الداخلة في تركيب معلقات وأقراص النِسْتاتين، كما جرى تحضير ثلاث محاليل تحتوي على النِسْتاتين بتركيز 100% من تركيز المعياري وأضيفت لها السواغات السابقة.
حُقنت خمس عينات متتالية من محلول معياري النِسْتاتين فكان RSD أقل من 2%، ثم حُقنت المحاليل المحضرة فلم يعطِ المحلول المحتوي على السواغات أي استجابة، بينما أعطت المحاليل الثلاثة الباقية استجابة، وحسبت الاستعادة فكانت 99.59 (5-8).
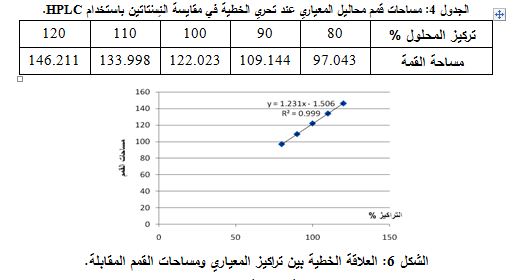
* الخطية والمجال Linearity and range:
حُضرت محاليل تراكيزها 80، 90، 100، 110، 120% من تركيز محلول المعياري، ثم حقنت المحاليل وسجلت مساحات القمم الموافقة (الجدول 4). بعد ذلك، رُسم الخط البياني بين التراكيز ومساحات القمم (الشكل 6)، فكان معامل الارتباط = 0.999 والعلاقة خطية (5-8).
* حد القياس الكمي Quantitation limit:
حُضرت سلسلة من المعياري بتراكيز متناقصة،
وقيس كل تركيز ست مرات، فكان حد القياس الكمي = + (10 × SD) X، حيث أن X هي متوسط الاستجابة لأقل تركيز بحيث يكون RSD أقل من 20 %: = QL 0.91 مكغ/ مل (5-8).
* حد الكشف Detection limit:
حُضرت سلسلة من معياري النِسْتاتين بتراكيـز متناقصة، وأعيد قياس المحلول الذي يعطي استجابة واضحة ومقبولة 6 مرات، فكان: DL = (SD × 3) + X = 0.7 مكغ/ مل (5-8).
* المتانة Robustness:
جرى تبديل تدفق الطور المتحرك زيادة ونقصان 0.1 مل/ د، ثم حقن محلول النِسْتاتين المعياري خمس مرات عند كل تدفق وحسب RSD، بعد ذلك حقن محلول المعلق ومحلول الأقراص بتركيز 100% من تركيز المعياري، فكانت جميع القيم ضمن معايير القبول (5-8).
|
| طريقة المقايسة بمقياس الطيف الضوئي بالأشعة فوق البنفسجية UV spectrophotometer assay: |
قياس الامتصاصية:
جرى القياس عند موجة طولها 305 نانومتر على UV-spectrophotometer، وباستعمال الميثانول لضبط نقطة بداية الامتصاص.
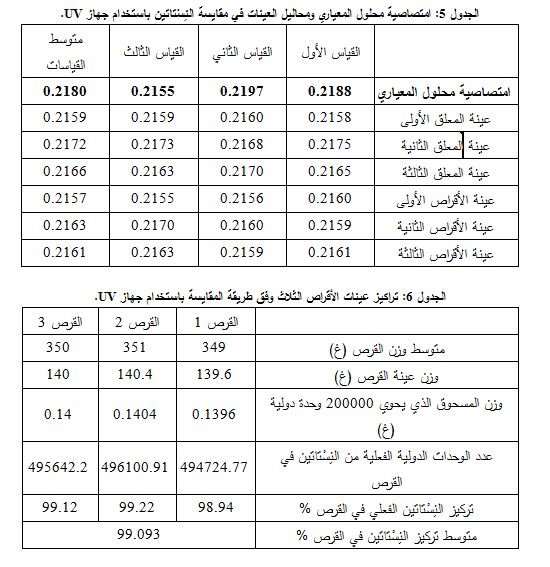
تُظهر الجداول 5 و6 و7 قيم الامتصاصية لمحلول المعياري ومحاليل العينات وتراكيز النِسْتاتين للعينات المدروسة باستخدام جهاز UV.
|
 |
| التحقق من مصدوقية الطريقة Method validation: |
* المضبوطية:
كانت قيمة قراءة امتصاصية المحلول المعياري للنِسْتاتين مساوية لـ 0.2182.
جرى تحضير ثلاث محاليل للنِسْتاتين تركيزها 80% من تركيز محلول المعياري، وثلاث محاليل تركيزها 100%، وثلاث محاليل تركيزها 120%، ثم قيست امتصاصية العينات عند موجة طولها 305 نانومتر، فكانت الاستعادة 98.943% (5، 6، 9، 10).
* الدقة:
- قابلية إعادة النتائج أو التناتج: قُرئت امتصاصية المحلول المعياري للنِسْتاتين فكانت قيمتها 0.2182.
أُخذ عينة من محلول النِسْتاتين ذي التركيز 100% من المعياري، وقيست امتصاصيتها ست مرات متتالية عند موجة طولها 305 نانومتر، ثم كرر قياس الامتصاصية ست مرات متتالية أيضاً في مختبر آخر، فكان RSD مساوياً لـ 0.24.
- التكرارية أو قابلية تكرار النتائج: قُرئت امتصاصية المحلول المعياري للنِسْتاتين فكانت قيمتها مساوية لـ 0.2182، ثم قيست امتصاصية عينة من محلول النِسْتاتين تركيزها 100% من المعياري تسع مرات متتالية، فكان RSD يساوي 0.41 (5، 6، 9، 10).
* النوعية:
حُضرت أربعة محاليل، بحيث يحتوي المحلول الأول على السواغات الداخلة في تحضير أقراص ومعلقات النِسْتاتين، بينما تحتوي المحاليل الثلاثة الباقية على النِسْتاتين بتركيز يساوي 100% من تركيز المعياري وأضيفت لها السواغات السابقة.
جرت قراءة امتصاصية العينات المأخوذة من المحاليل الأربعة المحضرة عند موجة طولها 305 نم، فكانت الاستعادة 99.81 (5، 6، 9، 10).
* الخطية والمجال:
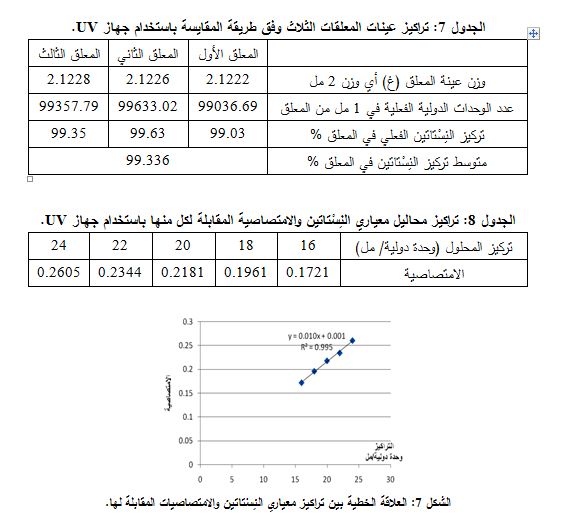
حُضرت محاليل تراكيزها 80، 90، 100، 110، 120 وحدة دولية / مل من تركيز المعياري، وقيست امتصاصيتها (الجدول 8(.
ثم رسم الخط البياني بين التراكيز والامتصاصية (الشكل 7) فكان معامل الارتباط = 0.995، فالعلاقة خطية، والمجال هو 16– 24 وحدة دولية/ مل (5، 6، 9، 10).
* حد الكشف:
جرت قراءة امتصاصية المحلول المعياري للنِسْتاتين فكانت قيمته 0.2182، ثم جرت قراءة امتصاصية محلول للنِسْتاتين بتركيز 100% من المعياري سبع مرات. بعد ذلك، حسب الانحراف المعياري SD للقراءات السبعة فكان مساوياً 0.215، وعندها طبقت العلاقة: LOD .T-Value = SD حيث T-Value = 3.143 عند تكرار القراءة سبع مرات، فكان حد الكشف 0.675 مكغ/ مل (11).
* حد القياس الكمي:
لحساب حد القياس الكمي طبقنا العلاقة التالية: SD×LOQ = 10 فكان مساوياً 2.15 مكغ/ مل (11).
* المتانة:
جرى تبديل طول موجة الامتصاص زيادة ونقصان 5 نانومتر، وقرىء امتصاص محلول النِسْتاتين المعياري ثلاث مرات عند كل طول موجة، ثم جرت قراءة امتصاص عينة المعلق وعينة الأقراص بتركيز 100% من المعياري فكانت القيم ضمن معايير القبول (5، 8).
|
 |
| المناقشة والتوصيات
Discussion and recommendations
|
تراوح زمن احتباس النِسْتاتين لدى مقايسته باستخدام HPLC بين 5.4-5.9 دقيقة، بينما كانت قيمته 3.5 دقيقة باستخدام HPLC أيضاً، وفق المرجع رقم 2، فالفارق بين زمني الاحتباس مهمل والطريقتان متقاربتان في النتائج، لذا يمكن استخدام عمود ODS-3 وطور متحرك مؤلف من ميثانول 70% + ماء 20% + 10 DMF% في المقايسة دون ظهور زيادة هامة في زمن الاحتباس.
جرى التحقق من مصدوقية طريقتي مقايسة النِسْتاتين. لكن طريقة المقايسة باستخدام جهاز HPLC كانت أكثر مضبوطية ودقة ونوعية وخطية ومتانة من طريقة المقايسة بوساطة UV- spectrophotometer، كما أن حد الكشف وحد القياس الكمي كانا أقل، لذا ينصح باستخدام HPLC وفي حال عدم توفره يمكن استخدام جهاز UV-spectrophotometer كبديل، والحصول على نتائج متشابهة.
وبالاعتماد على النتائج السابقة يوصى بما يلي:
1- الاعتماد على الطريقة الدستورية لمقايسة النِسْتاتين وهي طريقة المقايسة الحيوية، حيث تبقى هذه الطريقة معياراً لنفي أي شك محتمل لفقدان القوة، لعدم قدرة الطرق الكيميائية على إثبات ذلك.
2- متابعة تطوير طرق جديدة لمقايسة النِسْتاتين بكافة أشكاله الصيدلانية، حيث يعد من الأدوية الهامة المضادة للفطريات.
3- أعطت طريقة مقايسة النِسْتاتين بواسطة جهاز
HPLC نتائجَ تتمتع بالدقة والحساسية والنوعية لذا يمكن استخدامها لمقايسة النِسْتاتين في أشكاله الصيدلانية عندما نريد الحصول على نتائج سريعة.
4- إن طريقة مقايسة النِسْتاتين بواسطة UV-spectrophotometer غير مكلفة وغير مستهلكة للوقت، وأعطت نتائج قريبة من HPLC، لذا يمكن استخدامها في حال عدم توفر HPLC في المختبرات.
|
| المراجع References |
1-Charles R. Craig and Robert E. Stitzel
Antifungal drugs in Modern pharmacology with clinical applications.
Lippincott Williams & Wilkins, fifth edition, Chapter 52: 598-600, 2004.
2-Kay R. Bagon
The assay of antibiotics in pharmaceutical preparations using reverse-phase HPLC.
Journal of High Resolution Chromatography, 2, 5, 211-215, 2005.
3-Juan M. Llabot, Daniel A. Allemandi, Ruben H. Manzo, Marcela R. Longhi
HPLC method for the determination of nystatin in saliva for application in clinical studies.
J. of Pharmaceutical and Biomedical Analysis, 526-530, 2007.
4-British pharmacopeia BP, 2009.
5- أ.د. محمد عامر المارديني
كتاب المراقبة الدوائية، مطبوعات جامعة دمشق، 4، 615-652، 2008.
6-R. LoBrutto and T. Patel
Method validation.
HPLC for Pharmaceutical Scientists.
John Wiley & Sons, Inc, 455- 502. 2007.
7-Ashley S. Lister
validation of HPLC methods in pharmaceutical analysis.
Handbook of Pharmaceutical Analysis by HPLC, 2005: 191-217.
8-Chan C.C; Lam H; Lee Y.C. and Zhang X.M.
Analytical Method Validation and Instrument performance verification. Wiley Interscience, New York, 2004.
9-Robert A. Nash, Alfred H. Wachter
Validation of Analytical Methods and Processes
Pharmaceutical process validation, Second Edition, Marcel Dekker, Inc, 15: 542-559, 2003.
10-ICH Topic Q2B, guidance on validation of analytical procedures: Methodology.
The European Agency for the Evaluation of Medicinal Products, Human Medicines Evaluation Unit, 1996.
11-Analytical Detection Limit Guidance & Laboratory Guide For Determining Method Detection Limits, Wisconsin Department of Natural Resources Laboratory Certification Program, 1996.
|
| |
