| المجلد 6 ,
العدد 5
, جمادى الأولى 1433 - نيسان (أبريل) 2012 |
| |
| استخدام مقايسة الانترفيرون غاما في الدم الكامل لتشخيص السل الرئوي الفاعل |
| Use of Interferon-Gamma Assay in Whole blood
for Diagnosis of Active Pulmonary Tuberculosis |
| د. لين تقي الدين وأ. د. فوزة منعم |
| Lynn Taki-Eddin and Fawza Monem |
كلية الصيدلة، جامعة دمشق
Faculty of Pharmacy, Damascus University. |
| الملخص Abstract |
خلفية البحث: تعاني الطرق المخبرية المستخدمة في تشخيص مرض السل من مشاكل في الحساسية، النوعية، الكشف المبكر، الحصول على عينة ممثلة للآفة. ولقد توفر تجارياً اختبار جديد لتشخيص السل باستخدام مستضدات نوعية للمتفطرات السليةESAT-6 ، CFP-10، TB7.7 تحرّض إفراز الانترفيرون غاما(IFN-gamma) من اللمفاويات التائية المُحَسَّسة بشكل مسبق. صُممت هذه الدراسة لتجاوز هذه الصعوبات وتقييم إمكان استخدام مقايسة تحرر الانترفيرون غاماInterferon-Gamma Release Assay (IGRA) كمشعر تشخيصي لمرض السل الرئوي الفاعل.
الطرق: جرت مقايسة الانترفيرون غاما لدى 91 مريضاً يُشتبه بإصابتهم بالسل الرئوي الفاعل.
النتائج: ثبتت إصابة 48/91 (%52.7) مريضاً بالسل الرئوي الفاعل. وكانت حساسية IGRA تعادل %89.9، ونوعيتها %67.4، أما القيمة التنبؤية الإيجابية Positive predicted value (PPV) فكانت %75.4 والقيمة التنبؤية السلبية Negative predicted value (NPV) %85.3.
الاستنتاج: أظهرت طريقة الـ IGRA في هذه الدراسة حساسية جيدة في الكشف عن السل، إلا أن PPV المنخفضة تؤكد ضرورة استخدامها بالمشاركة مع الطرق التشخيصية الأخرى. تبدي NPV العالية لطريقة الـ IGRA دوراً إضافيا لهذا الاختبار في استبعاد العدوى بالسل الفاعل.
|
Background: Sensitivity, specificity, early confirmation and obtaining a representing specimen are challenging problems in tuberculosis diagnosis. A new diagnostic test for tuberculosis (TB) infection was commercially developed using specific Mycobacterium tuberculosis (MTB) antigens ESAT-6, CFP-10 and TB7.7 which induce interferon-gamma (IFN-gamma) from previously sensitized T cells. This study was designed to address these challenges and assess the potential of Interferon-Gamma Release Assay (IGRA) as a diagnostic indicator of active pulmonary TB.
Methods: Interferon gamma assay was performed in 91 patients with suspicion of pulmonary active tuberculosis.
Results: Active pulmonary TB was proved in 48/91 (52.7%) patients. Sensitivity, specificity, positive predicted value (PPV), and negative predicted value (NPV) were 89.9%, 67.4%, 75.4%, 85.3% for IGRA.
Conclusion: IGRA was a sensitive method in detecting TB, but its low PPV necessitated its use in combination with other methods. High NPV of IGRA for the diagnosis of active TB proposed an additional role of this test to exclude the infection with active TB.
|
| المقدمة Introduction |
يعد مرض السل واحداً من أهم الأسباب الإنتانية للمرض والوفيات في العالم. في عام 2009، قُدِّر حدوث 9.4 مليون إصابة جديدة، و 1.7 مليون حالة وفاة تقريباً بسبب السل (1). إن التشخيص السريع والدقيق أمر أساسي في العناية بمرضى السل والحد من انتقال هذا المرض (2). وعلى الرغم من النوعية الكبيرة للكشف المباشر عن العامل الممرض، مازال تشخيص السل يعاني من عقبات تقنية عدة: مثل تأخر النتائج، الصعوبة في الحصول على عينات ملائمة واعتماد بعض الطرق على المهارات الشخصية والعامل الشخصي.
هنالك فحص تشخيصي مناعي تأكيدي سريع وجديد للكشف عن الإصابة بعدوى السل، متوفر تجارياً، يعتمد على مقايسة تحرر الانترفيرون غاما interferon gamma release assay (IGRA). وتعتمد هذه الطريقة على أن اللمفاويات التائية المتحسسة للمستضدات السلية ستنتج الانترفيرون غاما IFN-γ عندما تتعرض مرة أخرى للمستضدات المتفطرية في المختبر؛ ويُفترض أن إنتاج كميات كبيرة من IFN-γ يرتبط بوجود عدوى السل (3). تستعمل هذه المقايسة مستضد early secretory antigen target 6 (ESAT-6) وculture filtrate protein 10 (CFP-10). يُرمّز كلا البروتينين بوساطة جينات تتوضع في منطقة الاختلاف 1 region of difference 1 (RD1) ضمن جينوم المتفطرات السلية Mycobacterium tuberculosis والتي تكون غير موجودة في M. bovis BCG ومعظم المتفطـرات غير السـلية nontuberculous mycobacterias NTM باستثناءM. sulzgai ، M. marinum و M. kansasii. بالإضافة إلى هذه المستضدات يُستخدم TB7.7 الذي تُرمّزه منطقة phage-inserted region (phiRv2) وهي ذات نوعية كبيرة للمتفطرات السلية (4).
تهدف دراستنا إلى تقييم إمكان استخدام طريقة الـ IGRA كمشعر جديد وواعد في تشخيص السل الرئوي الفاعل.
|
| المواد والطرق Materials and Methods |
جرت الدراسة على 91 مريضاً يشتبه بإصابتهم بالسل الرئوي الفاعل، كانوا من مراجعي المركز التدريبي لمكافحة السل في دمشق ومن المقيمين في شعبة الصدرية في مستشفى الأسد الجامعي في دمشق، خلال الفترة الواقعة ما بين شهري كانون الثاني وأيلول 2010، حيث أُخِذت موافقتهم بعد الحصول على توقيعهم على استمارة الموافقة المستنيرة لكل منهم. بُزلت عينات الدم الوريدي، واستُخدمت عتيدة QuantiFERON-TB Gold In-Tube (QFT-GIT) لمقايسة الانترفيرون غاما وأنبوبي QFT-GIT لجمع الدم من كل مريض Nil Control and TB Antigen tubes المنتج من قبل شركة Cellestis Ltd, Victoria, Australia وفق تعليمات الشركة المصنِّعة. جرى قياس الكثافة البصرية optical density باستخدام قارئ Sunrise Remote microplate reader (Tecan, Austria) مُهيّأّ على مرشحة 450 نانومتر ومرشحة مرجعية 690 نانومتر. اعتُبرت النتائج الأعلى من القيمة الحديّة 0.35 IU/ml كنتائج إيجابية.
أُخذ التشخيص النهائي من ملفات المرضى الطبية، واعتمد على نتائج الفحص السريري، التصوير الشعاعي، الدراسة الجرثومية، والتشريح المرضي. جرت الدراسة الإحصائية باستخدام معامل الارتباط Kendall's tau-b من أجل دراسة علاقة الارتباط بين التشخيص النهائي وطريقة الـ IGRA، واعتبرت قيمة P-value<0.05 معتداً بها إحصائياً، واستُعمل حدي الثقة 95% Confidence intervals CI.
|
| النتائج Results |
أُخذت نتائج التشخيص النهائي من ملفات المرضى الطبية (n=91)، فتبين من خلال الفحوصات والتقصيات السريرية للأطباء، بمعزل عن المقايسة المخبرية التي أجريت في هذه الدراسة، بأن 48/91 عينة (52.7%) شُخّصت إصابتهم بالسـل، وأما البقية 43/91 (47.3%) فلقد توزع تشخيصهم السريري كالتالي: (43/12) إنتانات تنفسية، (3/34) ربو، (543/) مصابون بالداء الرئوي المسدّ المزمن COPD، (43/2) COPD مترافق مع إنتانات مزمنة، (43/5) سرطانة، (43/1) سرطانة مترافقة مع ذات رئة، (43/1) توسع قصبي، (43/1) قصور تنفسي، (43/1) السحار السيليسيّ، (43/1) خثار الأوردة العميق-انصمام رئوي، (43/5) تليف رئوي، (43/3) ذات رئة، (43/1) داء البروسيلات، (43/1) داء الرشاشيات الرئوي، (43/1) قصور قلبي.
عند إجراء اختبار الـ IGRA كان إيجابياً في 57/91 عينة (62.6%)، 57/43 حالة ثبتت إصابتهم بالسل والـ 14 حالة المتبقية كانت عند مرضى أظهر تشخيصهم النهائي بأنهم غير مصابين بالسل. بالمقابل كانت طريقة الـ IGRA سلبية في 34/91 عينة (37.4%)، 34/5 حالة كانت لدى مرضى مصابين بالسل المُشخص سريرياً، فكانت نوعية هذا الاختبار وحساسيته 67.4% (57.77-77.2، 95%CI) و89.9% (83.58-96.21، 95%CI)، على الترتيب. وكانت القيمة التنبؤية الإيجابية Positive predictive value (PPV) والقيمة التنبؤية السلبية Negative predictive value (NPV) 75.43% (66.4-84.45،95%CI)، 85.29% (77.86-92.71، 95%CI)، على الترتيب (الشكل 1).
عند دراسة الارتباط بين طريقة الـ IGRA والتشخيص النهائي باستعمال معامل الارتباط كيندال Kendall's tau-b، أبدت هذه الطريقة ارتباطاً مع التشخيص النهائي، حيث كانت قيمة P-value تشير إلى علاقة يُعتد بها إحصائياً (P-value< 0.05).
|
| المناقشةDiscussion |
ظهرت السلبية الكاذبة للـ IGRA عند مريضين مصابين بالسل كانا يعانيان من المرض بطوره الحاد، مما يدل على أن تقدم المرض يمكن أن يؤدي إلى إضعاف استجابة الخلايا التائية (5)، أو يمكن أن يكون ذلك بسبب خلل وراثي في جهازهما المناعي كعدم القدرة على إنتاج كميات كافية من الـ IFN-γ. في هذه الحالة يمكن الاستعانة بأنبوب الـ mitogen الذي يُزوَّد بشكل اختياري مع عتيدة الـ IGRA ويستخدم كشاهد لتقييم الاستجابة المناعية وإنتاج الـ IFN-γ. أبدت الـ IGRA نوعية منخفضة في تشخيص السل الرئوي الفاعل مقارنة مع الدراسات المنشورة سابقا (6-8). ويمكن أن تُفسر هذه النوعية المنخفضة بأن طريقة الـ IGRA غير قادرة على التمييز بين عدوى السل الكامنة والفاعلة (9)، لذلك يمكن اعتبار نتائج الـ IGRA الإيجابية عند 14 مريضاً غير مصاب بالسل على أنها تدل على إصابتهم بالسل الكامن، حيث كان لديهم واحد أو أكثر من عوامل الاختطار للإصابة بعدوى السل، بالإضافة إلى أنهم مقيمين في سورية التي تعد منطقة عالية الوبائية بمرض السل (10). بالإضافة إلى ذلك وحيث أن طبيعة هذه الدراسة هي تقييم قدرة الـ IGRA على تشخيص السل الفاعل، خلال الممارسة السريرية الروتينية، لذلك فإن المرضى الذين اشتركوا في الدراسة هم مرضى يشتبه بإصابتهم بالسل، بينما تضمنت الدراسات الأخرى أشخاص أصحاء كشواهد سلبية ومرضى مشخصين مسبقاً بالسل كشواهد إيجابية وبالتالي كانت النوعية في دراستنا أقل (11). مع ذلك، فإنه يمكن للمرضى إيجابيي الـ IGRA أن يكون لديهم اختطار تطور السل الكامن إلى سل فاعل وبالتالي فإنهم يحتاجون إلى المزيد من الاستقصاءات والمتابعة.
يزيد الكبح المناعي الناتج عن العداوى، أو استخدام العوامل الحيوية، مثل أضداد ضد عامل النخر الورمي ألفا anti-tumor necrosis factor alpha antibodies، من إعادة تفعيل عدوى السل الكامن. لذلك قد تكون اختبارات المسح للسل الكامن بطريقة الـ IGRA مفيدة جداً في مثل هذه الحالة (5) وكذلك في حالة المرضى المصابين بفيروس العوز المناعي البشري HIV الذين لديهم تعداد خلايا CD4 T أكثر من 250 كرية/ مم3 (12). كما يمكن أن تؤدي العدوى بمتفطرات أخرى غير سلية M. kansasii، M. szulgai، M. marinum إلى نتائج إيجابية كاذبة (13).
|
| الاستنتاج Conclusion |
| أظهرت طريقة الـ IGRA حساسية جيدة في الكشف عن السل الرئوي الفاعل، إلا أن قيمتها التنبؤية الإيجابية تدل على ضرورة استخدامها بالمشاركة مع الطرق الأخرى لتشخيص السل الفاعل. ويمكن أن تكون مفيدة أكثر في المناطق التي يكون فيها السل الكامن قليل الانتشار. إن القيمة التنبؤية السلبية العالية للـ IGRA في تشخيص السل الرئوي الفاعل تعطي دوراً إضافياً لهذا الاختبار في استبعاد العدوى بالسل الفاعل. |
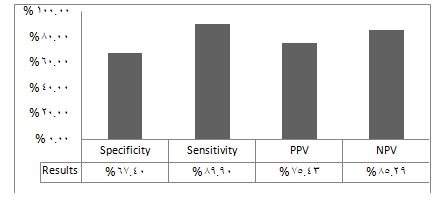
الشكل 1: مقايسة تحرر الانترفيرون غاما: حساسيتها، نوعيتها، القيم التنبؤية الإيجابية (PPV )، والسلبية (NPV ) لدى المرضى المشتبه بإصابتهم بالسل مقارنةً مع التشخيص السريري النهائي (أُخِذ من ملفات المرضى الطبية).
|
| المراجع References |
1-World Health Organization.
Global tuberculosis control 2010. Switzerland: WHO Press, 2010.
2-World Health Organization.
Diagnostics for tuberculosis: global demand and market potential. Switzerland: WHO Press, 2006
3-Ritacco W, Cardoso S. and Palomino JC.
New developments and perspectives. In Palomino JC, Le?o SC, Ritacco V, editors. Tuberculosis 2007: from basic science to patient care, First Edition.
http://www.tuberculosistextbook.com/index.htm. 661-680, 2007.
4-Leyten EM, Mulder B, Prins C, Weldingh K, Andersen P, Ottenhoff TH, van Dissel JT. and Arend SM.
Use of enzyme-linked immunospot assay with Mycobacterium tuberculosis-specific peptides for diagnosis of recent infection with M. tuberculosis after accidental laboratory exposure.
J Clin Microbiol; 44 (3): 1197-1201, 2006.
5-Ravn P, Munk ME, Andersen AB, Lundgren B, Lundgren JD, Nielsen LN, Kok-Jensen A, Andersen P. and Weldingh K.
Prospective evaluation of a whole-blood test using Mycobacterium tuberculosis-specific antigens ESAT-6 and CFP-10 for diagnosis of active tuberculosis.
Clin Diagn Lab Immunol; 12 (4): 491-496, 2005.
6-Kalantri Y, Hemvani N. and Chitnis DS.
Evaluation of whole blood IFN? test using PPD and recombinant antigen challenge for diagnosis of pulmonary and extra-pulmonary tuberculosis.
Indian J Exp Biol; 47 (6): 463-468, 2009.
7-Lee JY, Choi HJ, Park IN, Hong SB, Oh YM, Lim CM, Lee SD, Koh Y, Kim WS, Kim DS, Kim WD. and Shim TS.
Comparison of two commercial interferon-gamma assays for diagnosing Mycobacterium tuberculosis infection.
Eur Respir J; 28 (1): 24-30, 2006.
8-Mori T, Sakatani M, Yamagishi F, Takashima T, Kawabe Y, Nagao K, Shigeto E, Harada N, Mitarai S, Okada M, Suzuki K, Inoue Y, Tsuyuguchi K, Sasaki Y, Mazurek GH. and Tsuyuguchi I.
Specific detection of tuberculosis infection: an interferon-gamma-based assay using new antigens.
Am J Respir Crit Care Med; 170 (1): 59-64, 2004.
9-Singh M. and Espitia C.
Immunological diagnosis. In Palomino JC, Le?o SC, Ritacco V, editors. Tuberculosis 2007: from basic science to patient care, First Edition.
http://www.tuberculosistextbook.com/index.htm. 401-424, 2007.
10-World Health Organization.
Global tuberculosis control 2009: epidemiology, strategy, financing. Switzerland: WHO Press, 2009.
11-Kang YA, Lee HW, Hwang SS, Um SW, Han SK, Shim YS. and Yim JJ.
Use fulness of whole-blood interferon-gamma assay and interferon-gamma enzyme-linked immunospot assay in the diagnosis of active pulmonary tuberculosis.
Chest; 132 (3): 959-965, 2007.
12-Rangaka MX, Wilkinson KA, Seldon R, Van Cutsem G, Meintjes GA, Morroni C, Mouton P, Diwakar1 L, Connell TG, Maartens G and Wilkinson RJ.
Effect of HIV-1 infection on T-Cell-based and skin test detection of tuberculosis infection.
Am J Respir Crit Care Med; 175 (5): 514-520, 2007.
13-Madariaga MG, Jalali Z. and Swindells S.
Clinical utility of interferon gamma assay in the diagnosis of tuberculosis.
J Am Board Fam Med; 20 (6): 540-547, 2007.
|
| |
| المجلد 6 ,
العدد 5
, جمادى الأولى 1433 - نيسان (أبريل) 2012 |
|
|
|
