| المجلد 7 ,
العددان 7-8
, رمضان 1436 - تموز (يوليو) 2015 |
| |
| دراسة مستويات الـNGAL للتنبؤ بالأذية الكلوية الحادة لدى أفراد سوريين |
| Study of NGAL Levels to Predict Acute Kidney Injury
in Syrian People
|
| د. لمى الخجا وأ. د. المعتصم بالله زيتون |
| Al khouja L. and Zetoune A. |
كلية الصيدلة، جامعة دمشق
Faculty of Pharmacy, Damascus University
|
| الملخص Abstract |
| الـ Neutrophil gelatinase associated lipocalin (NGAL) (المعروف أيضاً بـLipocalin 2 أو Lcn2) هو بروتين صغير الوزن الجزيئي (25 Kd) ينتمي لعائلة الـ Lipocalins التي تقوم بنقل المواد الصغيرة الكارهة للماء. ولقد أظهرت الدراسات فائدة مركبNGAL في تمييز الأذية الكلوية الحادة والمزمنة وفي التنبؤ بالأذية الحادة بعد 2-3 ساعات من حدوثها مقارنة مع الكرياتينين الذي يحتاج الى 2-3 أيام ليزداد تركيزاً. جرت مقايسة المستويات المصلية للـ NGAL والكرياتينين واليوريا والسكر لدى 80 مريضاً، قسموا إلى مجموعة مرضى الفشل الكلوي الحاد ومرضى الفشل الكلوي المزمن ومرضى الهجمة الكلوية الحادة بعد إصابتهم بفشل كلوي مزمن ومجموعة مرضى أُخذت منها العينات بعد الأذية الحادة بساعتين وبعدها بـ 3 أيام. وجدنا ارتفاعاً في مستويات NGAL لدى مجموعات المرضى مقارنة مع الشواهد، ووجدنا أيضاً مستويات NGAL عالية لدى المرضى الذين جُمعت عيناتهم بعد ساعتين من الأذية الحادة، بينما كانت قيم الكرياتينين واليوريا ضمن المجال السوي. لكن ارتفعت المتثابتات الثلاث في العينات المأخوذة بعد ثلاثة أيام. تبين هذه الدراسة أن مستويات NGAL المصلية تزداد في الأذية الكلوية الحادة ولهذا يمكن استخدام مستوى NGAL كواصم حيوي مبكر للتنبؤ بالأذية الكلوية الحادة المُبكرة وتشخصيها قبل بدء ارتفاع مستويات الكرياتينين واليوريا. |
The Neutrophil gelatinase associated lipocalin (NGAL) (also known as Lipocalin 2 or Lcn2) is a small molecule protein (25 Kd) and belongs to the family of the Lipocalins that transport small hydrophobic materials.
Studies have shown the benefit of NGAL in distinguishing the acute and chronic renal injury and prediction of acute renal injury after 2-3 hours of its occurrence compared with creatinine which takes 2-3 days to rise. Serum level of NGAL, creatinine, urea and sugar was measured in 80 patients, divided into group of patients with acute renal failure and patients group with chronic renal failure and patient group with acute renal attack after they had chronic kidney failure, and patients group of which samples were collected after two hours and 3 days from the occurrence of the acute injury.
We found high levels of NGAL in patient groups compared with the controls. We also found high levels of NGAL in patients whose sample were collected after two hours of the acute injury, while the values of creatinine and urea were within the normal range. However, the three parameters increased in samples taken after three days.
This study established that levels of serum NGAL increase in acute renal injury, and thus NGAL level can be used as an early biomarkerthat predicts acute renal injury and diagnoses it before the onset of elevation of creatinine and urea levels.
|
| المقدمة Introduction |
الفشل الكلوي الحاد هو تدهور مفاجئ في الوظيفة الكلوية بسبب نقص سرعة الترشيح الكبيبي وعادة ما يكون عكوساً خلال فترة أيام أو أسابيع (1).
حالياً جرى استبدال مصطلح الفشل الكلوي الحاد Acute Renal Failure (ARF) بمصطلح الأذية الكلوية الحادةAcute Kidney Injury (AKI) لأن الفشل الكلوي الحاد يعبر عن الفشل في وظيفة الكلية ولا يعطي إمكان انعكاس العملية على المستوى الجزيئي والبنيوي والكيمياء الحيوية التي تتميز بها متلازمة الأذية الكلوية الحادة (1).
يسبب الفشل الكلوي نقصاً في إطراح الفضلات الحاوية على النتروجين والتي تقاس عادة باليوريا، مما يسبب ارتفاعاً في تركيز اليوريا في االدم أو ما يسمى باليوريميا Uraemia. وتصنف اليوريميا إلى: قبل كلوية Prerenal، كلوية Renal، بعد كلوية Posrenal (2).
جرى في السنوات الأخيرة تطوير العديد من الواصمات الحيوية التي تقدم تحرياً أكثر سرعة ونوعية للفشل الكلوي الحاد والتي يعد الـ (NGAL) Neutrophil Gelatinase Associated Lipocalin أهمها (3، 4).
|
| NGAL |
إن NGAL واصم حيوي واعد في تحري الـ AKI، يُرمّز من قبل جين LCN2. وهو عبارة عن بروتين وزنه الجزيئي 25 kDa مكون من سلسلة تحوي 178 من الأحماض الأمينية وعادة ما يكون بشكل وحيد التماثر monomeric form (5).
وهو ينتمي إلى عائلة بروتينات تدعى الليبوكالينات وهي عبارة عن بروتينات صغيرة ترسلها الخلايا إلى الخارج كي تربط جزيئات كارهة للماء وتحملها إلى داخل الخلية. وتعد الجزيئات الحاملة للحديد siderophore اللجين الأهم لليبوكالينات (6).
يجري التعبير عن NGAL من قبل العدلات وغيرها مثل الخلايا الظهارية، بما فيها خلايا النبيب الداني (5).
يُحفّز إنتاجه تحت تأثير كل من: عديد السكاريد الشحمي الجرثومي LPS والديكساميتازون وعوامل النمو والسيتوكينات.
يقوم هذا البروتين بالتقاط جزيئات الحديد ونقلها الى داخل الخلية، مما يسبب زيادة المستويات الهيولية من الحديد. إن التفاعل مع الموقع الرابط للحديد يعطي مركب NGAL لونه المميز الأحمر اللماع ويتواسط معظم تأثيراته البيولوجية (6).
|
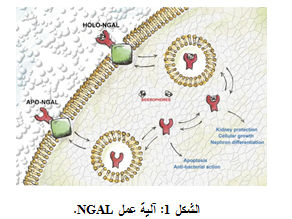
| آلية عمل NGAL |
بعد حدوث الأذية النسيجية تُفرز عوامل النمو والسيتوكينات التي تسبب تفعيل عامل الانتساخ kappa B (NF-kB) المسؤول عن نسخ جين LCN2، مما يسبب ارتفاع مستويات مركب NGAL.
يتفاعل مركب NGAL مع مستقبلاته الغشائية 24p3R, Megali (الشكل 1)، فبعد ارتباطه مع مستقبلاته، يدخل مركب NGAL إلى داخل الخلية إما كبروتين صميم وحيد (Apo-NGAL) أو كمعقد مع حاملات الحديد الرابطة للحديد (Holo-NGAL). وإن هذين الشكلين المختلفين مهمان جداً لأنهما يعطيان تأثيرات متعاكسة.
يُدخَل مركب Holo-NGAL إلى داخل حويصلات الجسيم الداخلي endosomal vesicles ويُنقَل ضمن المنطقة الهيولية، حيث يحرر معقد حديد- حامل الحديد، مما يسبب تفعيل طرق نوعية معتمدة على الحديد ضرورية لنمو الخلية وإصلاح الضرر، أما البروتين الحر فيجري تحطيمه أو إعادة إرساله إلى خارج الخلية (الشكل 1).
بينما يقوم مركب Apo-NGAL، بعد دخوله إلى داخل الخلية، بقبط الحديد الخلوي كالمغناطيس وتصديره إلى الفراغ خارج الخلوي مما يسبب نَفاد الحديد الخلوي، الأمر الذي يؤدي إلى الاستماتة Apoptosis تحت ظروف معينة (7، 8).
|
 |
| المواد والطرق Materials and Methods |
مجموعات الدراسة
شملت الدراسة 80 شخصاً وزعوا ضمن المجموعات التالية:
• مجموعة مرضى الفشل الكلوي الحاد.
• مجموعة مرضى الفشل الكلوي الحاد على أرضية مزمنة.
• مجموعة مرضى الفشل الكلوي المزمن.
• مجموعة أسوياء (شاهد).
جرى استبعاد العديد من المرضى الذين يعانون من حالات مرضية تؤثر على المتثابتات المدروسة بشكل كبير، أي المصابين بأي من الأمراض التالية: أمراض المناعة الذاتية، الأورام بأنواعها، الحمى الرثوية، الحوامل.
أخذت عينات مجموعات الدراسة من المستشفيات والمراكز التالية:
مستشفى المواساة (قسم الكلية والقلبية والعناية والإسعاف)، مركز جراحة القلب، مستشفى الأسد الجامعي (قسم الكلية والقلبية والإسعاف).
جُمعت عينات الدم خلال 8 أشهر في الفترة الواقعة بين 8 تشرين الأول عام 2013 وحتى 12 حزيران عام 2014 وذلك بعد تعبئة الاستمارة الخاصة ببيانات المرضى.
جمع العينات وحفظها وتنبيذها
بُزلت عينات الدم الصيامي (5 مل) لكل من المرضى والشواهد ضمن أنابيب جافة، ونبذت بسرعة 1000Xg بالدرجة 4+ ْC لمدة 15 دقيقة، وزّع المصل ضمن 3 أنابيب ايبندورف (500 مكل تقريباً في كل أنبوب) وحفظت بالدرجة80- ْC إلى حين إجراء المقايسة.
تجنبنا استخدام العينات الشحمية أو المنحلة بشدة أو اليرقانية لكونها تؤثر على دقة المقايسة.
جرت مقايسة الواصمات التالية: NGAL، الكرياتينين، اليوريا، السكر.
حيث عوير السكر لتبيان في ما إذا كان له علاقة مباشرة أو غير مباشرة بالأذية الكلوية الحادة أو المزمنة أو الحادة على أرضية مزمنة.
استخدمت الأجهزة التالية لإجراء المقايسات المختلفة: قارئ ELISA من نوع ABBOTT-tecan – sunrise, Germeny. وجهاز Specrtophotometer.
استخدمت عتائد المقايسات التالية:
مقايسة مركب NGAL: جرت المقايسة باستخدام عتيدة Human NGAL ELISA kit المصنعة من شركة SunRed الصينية CAT.NO.201-12-1720.
المبدأ: تستخدم مقايسة تقنية الممتز المناعي المرتبط بالإنزيم ذات الشطيرة Sandwich ELISA، فالصفيحة مغطاة مسبقاً بأضداد وحيدة النسيلة نوعية لمركب NGAL. تضاف المعياريات والعينات إلى الآبار، وبعد غسل أي مواد غير مرتبطة تُضاف الأضداد المعدة للكشف detection الموسومة بالبيوتين النوعية لعامل للـ NGAL إلى الآبار، تجري عملية غسل ثانية لإزالة أية أضداد موسومة بالبيوتين غير مرتبطة، يضاف بعد ذلك إلى الآبار الإنزيم المنضم إلى الستربتافيدين فيرتبط الإنزيم مع الأضداد الموسومة بالبيوتين، ثم يغسل مرة ثالثة. ومن ثم يضاف محلول الرَكيزَة إلى الآبار فيتطور لون متناسب مع كمية مركب NGAL المرتبط في الخطوة الأولى، يوقف تطور اللون بإضافة محلول الإيقاف، ثم تقاس شدة اللون الناتج.
مقايسة الكرياتينين: جرت مقايسة الكرياتينين باستخدام عتيدة مصنعة من شركة Spinreact الأسبانية.
المبدأ: تعتمد المقايسة على تفاعل الكرياتينين مع بكرات الصوديوم المعروف بتفاعل جافه Jaffe.
يتفاعل الكرياتينين مع البكرات القلوية مشكلاً معقداً أحمر اللون وتكون شدة اللون الناتج متناسبة مع تركيز الكرياتينين.
مقايسة اليوريا: جرت مقايسة اليوريا باستخدام عتيدة مصنعة من شركة Spinreact الأسبانية.
المبدأ: تُحلل اليوريا إنزيمياً إلى أمونيا NH4+ وثاني أوكسيد الكربون CO2.
تتفاعل شوارد الأمونيا مع الساليسيلات والهيبوكلوريت NaClO بوجود النتربروسيد كمحفز للتفاعل لتشكل الإندوفينول الأخضر.
مقايسة السكر: جرت مقايسة الغلوكوز باستخدام عتيدة مصنعة من شركة Audit Diagnostic corporation الإيرلندية.
المبدأ: مقايسة إنزيمية لونية على جهاز Hitachi911 الآلي.
|
| النتائج Results |
أولاً: دراسة الفروق في الواصمات الحيوية بين مجموعات الفشل الكلوي، حسب نوعه (حاد – مزمن – حاد على مزمن):
لدراسة هذه الفروق جرى استخدام الاختبارات الإحصائية اللامعلمية كاختبار كروسكال ولاس للمقارنة بين أكثر من مجموعتين، واختبار مان ويتني للمقارنة بين مجموعتين.
جرى إنشاء جدول كروسكال ولاس لاختبار الفروق في الواصمات الحيوية بين مجموعات الفشل الكلوي الثلاث. ولقد اتضح عدم وجود فروق ذات دلالة إحصائية في تركيز كل من الكرياتينين واليوريا والسكر بين مجموعات الفشل الكلوي الثلاث (حاد – مزمن – حاد على مزمن)، أي أن مستويات هذه الواصمات الحيوية متقاربة في حالات الفشل الكلوي، مما يدل على أنها مؤشرات مستقرة مع كافة حالات الإصابة بالفشل الكلوي.
أما بالنسبة لبروتين مركب NGAL فتبين وجود فروق ذات دلالة إحصائية في تركيزه بين مجموعات الفشل الكلوي الثلاث (حاد – مزمن – حاد على مزمن) أي أن مستوى بروتين الـ NGAL مختلف ومتقلب بين حالات الفشل الكلوي، مما يدل على أنه مؤشر غير مستقر مع كافة حالات الإصابة بالفشل الكلوي. ولتحديد المجموعة التي يعد فيها بروتين مركب NGAL مؤشراً مرتفعاً قمنا باختبار الفروق الثنائية بين المجموعات حسب اختبار مان ويتني كما يلي:
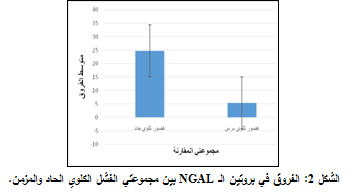
اختبار الفروق في بروتين NGAL بين مجموعتي الفشل الكلوي الحاد والمزمن:
تبين وجود فروق ذات دلالة إحصائية في تركيز بروتين NGAL بين مجموعة الفشل الكلوي الحاد ومجموعة الفشل الكلوي المزمن، لأن مستوى معنوية الاختبار البالغ 0.002 أصغر من مستوى الدلالة 0.01، وهذا الفرق كان لمصلحة مجموعة الفشل الكلوي الحاد، أي أن تركيز بروتين NGAL لدى مجموعة الفشل الكلوي الحاد كان أعلى من تركيزه لدى مجموعة الفشل الكلوي المزمن بفارق كبير ومعنوي. وهذا يدل على أن بروتين NGAL يعد مؤشراً حيوياً هاماً للإصابة بالفشل الكلوي الحاد ومؤشراً أقل أهمية للإصابة بالفشل الكلوي المزمن كما هو مبين في الشكل 2.
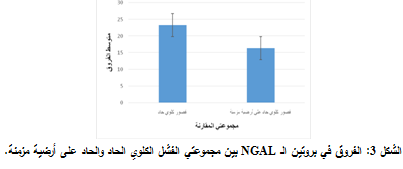
اختبار الفروق في بروتين NGAL بين مجموعتي الفشل الكلوي الحاد والحاد على أرضية مزمنة:
تبين عدم وجود فروق ذات دلالة إحصائية في تركيز بروتين NGAL بين مجموعة الفشل الكلوي الحاد ومجموعة الفشل الكلوي الحاد على أرضية مزمنة، لأن مستوى معنوية الاختبار البالغ 0.259 أكبر من مستوى الدلالة 0.01، أي أن تركيز بروتين NGAL لدى مجموعة الفشل الكلوي الحاد يتطابق مع تركيزه لدى مجموعة الفشل الكلوي الحاد على أرضية مزمنة وهذا يدل على أن بروتين NGAL يعد مؤشراً حيوياً هاماً للإصابة بالفشل الكلوي الحاد وللإصابة بالفشل الكلوي الحاد على أرضية مزمنة (الشكل 3).
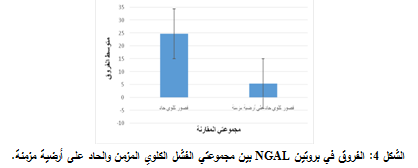
اختبار الفروق في بروتين NGAL بين مجموعتي الفشل الكلوي المزمن والحاد على أرضية مزمنة:
تبين وجود فروق ذات دلالة إحصائية في تركيز بروتين NGAL بين مجموعة الفشل الكلوي المزمن ومجموعة الفشل الكلوي الحاد على أرضية مزمنة، لأن مستوى معنوية الاختبار البالغ 0.009 أصغر من مستوى الدلالة 0.01 وهذا الفرق كان لمصلحة مجموعة الفشل الكلوي الحاد على أرضية مزمنة، أي أن تركيز بروتين NGAL لدى مجموعة الفشل الكلوي الحاد على أرضية مزمنة كان أعلى من تركيزه لدى مجموعة الفشل الكلوي المزمن بفارق كبير ومعنوي.
وهذا يؤكد على أن بروتين NGAL يعد مؤشراً حيوياً هاماً للإصابة بالفشل الكلوي الحاد على أرضية مزمنة ومؤشراً أقل أهمية للإصابة بالفشل الكلوي المزمن (الشكل 4).
اختبار الفروق في بروتين NGAL بين مجموعتي الفشل الكلوي المزمن الأسوياء:
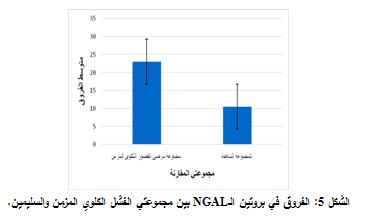
بما أن معدل تركيز بروتين NGAL لمجموعة المصابين بفشل كلوي مزمن كان قريباً من المعدل الطبيعي لمجموعة الأسوياء، جرى اختبار الفرق بينهما في تركيز بروتين NGAL وفي تركيز باقي الواصمات الحيوية موضوع البحث. ولقد تبين وجود فروق ذات دلالة إحصائية في تركيز كل من الكرياتينين واليوريا وبروتين NGAL بين مجموعة الفشل الكلوي المزمن ومجموعة السليمين لأن مستوى معنوية الاختبار البالغ 0.001 أصغر من مستوى الدلالة 0.01 لكل من هذه الواصمات الحيوية, وهذا الفرق كان لمصلحة مجموعة الفشل الكلوي المزمن، أي أن تركيز هذه الواصمات الحيوية لدى مجموعة الفشل المزمن كان أعلى من تركيزه لدى مجموعة السليمين بفارق معنوي.
وهذا يؤكد على أن هذه الواصمات الحيوية تعد مؤشرات حيوية للإصابة بالفشل المزمن، لكن بدرجة أقل من الأهمية مقارنة مع حالة الفشل الكلوي الحاد والفشل الكلوي الحاد على أرضية مزمنة (الشكل 5).
أما بالنسبة للواصم السكر فلا يعد مؤشراً حيوياً للإصابة بأي نوع من أنواع الفشل الكلوي، حيث لا يوجد فروق ذات دلالة إحصائية في تركيز السكر بين مجموعة الفشل الكلوي المزمن ومجموعة السليمين لأن مستوى معنوية الاختبار البالغ 0.057 أكبر من مستوى الدلالة 0.01.
ثانياً: دراسة الواصمات الحيوية لمجموعة التنبؤ للإصابة بالفشل الكلوي الحاد قبل الإصابة وبعدها: أُخذت العينات من المرضى الذين لديهم عامل اختطار لتطوير فشل كلوي حاد بعد ساعتين وبعد 3 أيام من احتمال الإصابة وذلك لتأكيد في ما إذا كان NGAL مشعراً تشخيصياً مبكراً للإصابة بالفشل الكلوي مقارنة باليوريا والكرياتينين. ولقد جرى اختيار العينات اعتماداً على رأي الأطباء وحالة المريض السريرية.
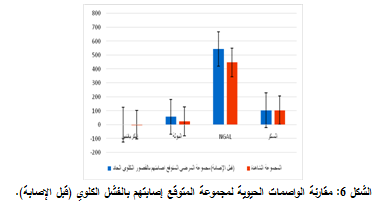
دُرست الإحصائيات الوصفية للواصمات الحيوية لمجموعة التنبؤ بالإصابة بالفشل الكلوي بعد ساعتين من الإصابة، أي قبل تشخيص الإصابة بارتفاع قيمة الكرياتينين واليوريا وتبين أن معدلات تركيز كل من الكرياتينين والسكر (0.88 و104.4 مغ/دل، على الترتيب) كانت ضمن الحدود الطبيعية (0.83 و104.5 مغ/دل، على الترتيب). أما اليوريا (57.4 مغ/دل) فلقد ارتفعت قليلاً عن الحدود السوية (24.0 مغ/دل). بالمقابل نجد أن بروتين NGAL قد ارتفع بشكل ملحوظ (544.5675 نغ/مل) مقارنة بالحدود السوية (447.5 نغ/مل) (الشكل 6).
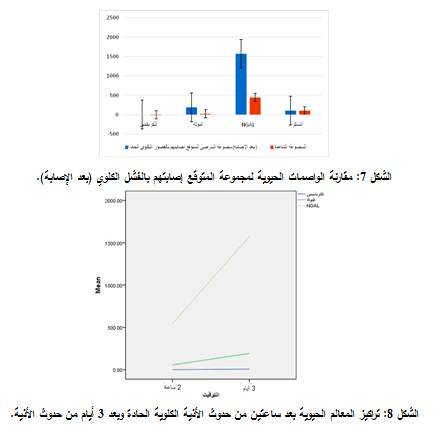
كما تمت دراسة الإحصائيات الوصفية للواصمات الحيوية لمجموعة التنبؤ بالإصابة بالفشل الكلوي بعد 3 أيام من الإصابة، أي بعد تشخيص الإصابة بارتفاع الكرياتينين واليوريا، حيث تبين أن معدلات تركيز كل من الكرياتينين (7.302 مغ/دل) واليوريا (192.34 مغ/دل) والـNGAL (1575.1268 نغ/مل) ارتفعت عن الحدود السوية بشكل كبير (0.83 مغ/دل، (57.4 مغ/دل، (447.5 نغ/مل، على الترتيب) أما تركيز السكر (103.8 مغ/دل) فكان ضمن الحدود السوية (104.5 مغ/دل) (الشكلان 7 و8).
كما قمنا باختبار الفروق في المعالم الحيوية لمجموعة التنبؤ للإصابة بالفشل الكلوي الحاد قبل الإصابة وبعدها تبين وجود فارق يُعتد به إحصائياً في تركيز كل من الكرياتينين واليوريا وبروتين NGAL لمجموعة التنبؤ للإصابة بالفشل الكلوي الحاد بين ما قبل الإصابة وما بعدها، لأن مستوى معنوية الاختبار البالغ0.043 أصغر من مستوى الدلالة 0.05 لكل من هذه الواصمات الحيوية، وهذا الفرق كان لمصلحة مجموعة التنبؤ للإصابة بالفشل الكلوي الحاد بعد الإصابة. أما بالنسبة للسكر فلم تكن هنالك فروق يُعتد بها إحصائياً في تركيزه لمجموعة التنبؤ قبل الإصابة وبعدها.
|
|
| المناقشة Discussion |
أظهرت الدراسة زيادة أفضل في ارتفاع تركيز NGAL المصلية لدى مرضى الفشل الكلوي الحاد، والمزمن، والحاد على أرضية مزمنة، ولكن مستوياته كانت الأعلى لدى مرضى الفشل الكلوي الحاد، والحاد على أرضية مزمنة، وبالتالي فإن واصم بروتين NGAL يعد مؤشراً حيوياً هاماً للإصابة بفشل كلوي حاد وللإصابة بفشل كلوي حاد على مزمن، وأنه مؤشر أقل أهمية للإصابة بفشل كلوي مزمن مقارنة بالفشل الكلوي الحاد وبالفشل الكلوي الحاد على أرضية مزمنة. ولقد توافقت النتائج مع نتائج دراسة Bolignano وزملائه عام 2009 (9) ودراسة Hazem وزملائه عام 2011 (10)، بينما كانت مخالفة لنتائج دراسة Breidthardt وزملائه عام 2012 (11).
يعزى ذلك إلى أن الخلايا الكلوية المتخربة في الإصابة الحادة أدت إلى إفراز كبير للبروتين مما سبب زيادة كبيرة في قيمه المصلية، أما عند تحول الفشل إلى الحالة المزمنة فإن الأذية الكلوية استقرت، وبالتالي لا يوجد خلايا متأذية جديدة تقوم بإفراز NGAL. إن ارتفاع الواصم في حالة الإصابة بالفشل الكلوي المزمن قد يعزى إلى أن الخلايا المتخربة المتبقية هي التي تسبب إفراز NGAL وعند استقرار حالة الكلية عند الازمان لا يكون الإفراز كبيراً.
كما أظهرت الدراسة أيضاً أن مستويات NGAL
قد ازدادت بعد ساعتين من حدوث الأذية الكلوية بينما بقيت مستويات الكرياتينين واليوريا ضمن الحدود الطبيعية، لكنها عادت وازدادت بعد 3 أيام من حدوث الأذية. وهذا يؤكد أهمية NGAL في التنبؤ المبكر بالإصابة بالفشل الكلوي الحاد وبالتالي إمكان تفادي حدوث إصابة دائمة في الكلية وتوافقت هذه النتائج مع نتائج دراسة Maisel وزملائه عام 2011 (12).
تبين أيضاً أن تركيز السكر المصلي لم يكن له أي دور يذكر أو أية علاقة مباشرة أو غير مباشرة في أي من مراحل الدراسة السابقة وبالتالي فهو لا يعد مؤشراً حيوياً للإصابة بالفشل الكلوي.
|
| الاستنتاج Conclusion |
| ينصح باستخدام مقايسة NGAL في تشخيص الفشل الكلوي الحاد والحاد على أرضية مزمنة والمزمن، والاستفادة منه كواصم حيوي مبكر تزداد مستوياته المصلية قبل ارتفاع الكرياتينين واليوريا وذلك للتنبؤ بالفشل الكلوي الحاد وبالتالي تجنب حدوث مضاعفات قد تودي بحياة المريض. |
| المراجع References |
1- Devarajan P.
Neutrophil gelatinase-associated lipocalin: a promisingbiomarker for human acute kidney injury.
Biomark Med, 2010, 4(2): 265-280.
2- Kumar P. and Clark M.
Renal disease.
In: Clinical Medicine. 6th Ed, Saunders Elsevier, 2005, 659-665.
3- Devarajan P.
Proteomics for biomarker discovery in acute kidney injury.
Semin Nephrol, 2007, 27: 637-651.
4- Devarajan P, Parikh C. and Barasch J.
Case 31-2007: a man with abdominal pain and elevated creatinine.
N Engl J Med, 2008, 358(3): 312.
5- Haukins R. and Korean.
J Lab Med, 2011, 31: 72-80.
6- Schmidt-Ott KM, Mori K, Li JY, et al.
Dual action of neutrophil gelatinase-associated lipocalin. Comprehensive review of the functional roles of NGAL.
J Am SocNephrol, 2007, 18:407-413.
7- Devireddy LR, Gazin C, Zhu X, Green MR.
A cellsurface receptor for lipocalin 24p3 selectively mediates apoptosis and iron uptake.
Cell, 2005, 123: 1293-1305.
8- Schmidt-Ott KM, Mori K, Li JY et al.
Dual action of neutrophil gelatinase-associated lipocalin.
J Am SocNephrol, 2007, 18: 407-413.
9- Bolignano D, Lacquaniti A, Coppolino G, Donato V, Campo S , Fazio MR, Nicocia G and Buemi M.
Neutrophil Gelatinase-Associated Lipocalin (NGAL) and Progression of Chronic Kidney Disease.
Clin J Am SocNephrol, 2009, 4: 337-344.
10- Hazem A, Bakry S, Obaia E, Gengehy S. and Mohamed W.
Serum and urinary NGAL in Acute and Chronic Kidney Disease.
JPBMS, 2011, 4 (13).
11- Breidthardt T, Socrates T, Drexler B, Noveanu M, Heinisch C, Arenja N, Klima T, Züsli C, Reichlin T, Potocki M, Twerenbold R, Steiger J. and Mueller C.
Plasma neutrophil gelatinaseassociated lipocalin for the prediction of acute kidney injury in acute heart failure.
Critical Care, 2012, 16:R2.
12- Maisel A, Mueller C, Fitzgerald R,Brikhan R, Hiestand B, Iqbal N, Clopton P and Veldhuisen D.
Prognostic utility of plasma neutrophil gelatinaseassociatedlipocalin in patients with acute heart failure: The NGAL EvaLuation Along with B-type NaTriuretic Peptide in acutely decompensated heart failure (GALLANT) trial.
European Journal of Heart Failure, 2011, 13, 846-885.
|
| |
| |
| المجلد 7 ,
العددان 7-8
, رمضان 1436 - تموز (يوليو) 2015 |
|
|
|
