| المجلد 7 ,
العددان 9-10
, ربيع الثاني 1437 - كانون الثاني (يناير) 2016 |
| |
| ترافق طفرات الجِيْنَيْن GJB6 وGJB2 لدى مرضى سوريين يعانون من فقد السمع الخِلْقي المتنحي غير المرافق للمتلازمات |
| Coexistence of GJB6 and GJB2 Mutations in Syrian Patients with Congenital Recessive Non-syndromic Hearing Loss |
| د. طارق زيدية وأ. د. فوزة منعم |
| Tarek Zaidieh1, Fawza Monem1,2 |
1 كلية الصيدلة، جامعة دمشق، 2 مستشفى الأسد الجامعي، جامعة دمشق
1Faculty of Pharmacy, 2Al-Assad University Hospital, Damascus University
|
| الملخص Abstract |
| مازالت الدراسات المعنية بفقد السمع الخِلْقي لدى السكان السوريين في بداياتها، ولا توجد حتى الآن معلومات واضحة عن تواتر الطفرات المسبِّبة باستثناء طفرات جين GJB2. هدفت دراستنا إلى تقدير مدى ترافق طفرات جين GJB6 مع طفرات جين GJB2 لتصميم خطة فعالة للتشخيص الجزيئي والمشورة الوراثية. جرى تحري طفرات جين GJB6 بواسطة تفاعل PCR لدى 41 مريضاً يعانون من فقد السمع الخلقي المتنحي غير المرافق للمتلازمات الذين دُرست لديهم سابقاً طفرات الإكسون الثاني من جين GJB2. لم نلاحظ أيّ ترافق بين طفرات الجينين GJB2 وGJB6، حيث كُشفت طفرة del (GJB6-D13S1830) بشكل متماثل الزيجوت homozygous لدى حالة واحدة من ذوي نمط جين GJB2 الشائع wild type (2.9%). إنّ الاقتصار في تحري هذه الطفرة على المرضى متغايري الزيجوت heterozygous لطفرات GJB2 لا يضمن كفاءة التشخيص الجزيئي وكفاية المشورة الوراثية في مجتمعنا. |
| Research studies of congenital hearing impairment in the Syrian population are still in their infancy. Till now, No clear data about the causative mutations except GJB2 mutations are available. Our study aimed to estimate the coexistence of GJB6 and GJB2 mutations, in order to validate an efficient procedure for molecular diagnosis and genetic counseling. GJB6 mutations were screened by PCR in 41 patients with congenital recessive non-syndromic hearing loss patients who were previously analyzed for GJB2 exon 2 mutations. Coexistence of GJB2 and GJB6 mutations was not encountered, as del(GJB6-D13S1830) was found in homozygosity in only one case with a wild type GJB2 gene (2.9%). Efficiency of molecular diagnosis and genetic counseling does not seem guaranteed in our population when screening for del(GJB6-D13S1830) is confined to heterozygotes for a GJB2 mutation. |
| المقدمة Introduction |
يعد فقد السمع الخلقي من أكثر الإعاقات الحسية انتشاراً (1) وتُعدّ الطفرات الجينية غير المسبّبة للمتلازمات العامل المسؤول عن ثلث الحالات تقريباً (2). إلى يومنا هذا جرى تحديد أكثر من 70 موقعاً جينياً مرتبطاً بفقد السمع الخلقي المتنحي غير المرافق للمتلازمات (3)، ولكن تبقى طفرات جين GJB2 المرمّزة للبروتين كونكسين 26 في الموقع DFNB1 هي الأكثر تواتراً (50%) في هذه الحالات (4)، حيث جرى كشف أكثر من 90 طفرة، يتوضّع معظمها في الإكسون الثاني من جين GJB2 (5). ويجدر الذكر أن الصمم يبقى غير مفسّر لدى 10-50% من هؤلاء المرضى لأنّ لديهم أليلاً طافراً واحداً فقط يحمل واحدة من طفرات جين GJB2 مثل (35delG, 176delT,W77R, R184,......) (6).
ثمة جين أخر ضالع في النمط المتنحي من الصمم الخلقي تتوضع على الذراع الطويل للصبغي 13 في المنطقة 12 13q12)) وعلى بُعد 35 ألف زوج قاعدي من جين GJB2 تدعى جين GJB6 ترمّز البروتين كونكسين 30، حيث كشفت فيها طفرتا حذف، الأولى [del(GJB6-D13S1830) بطول 309 kb] لدى 50% من المرضى متغايري الزيجوت بالنسبة لطفرات GJB2 بنمط زيجوت متغاير مزدوج double heterozygous (7،8)، والثانية [del(GJB6-D13S1854) بطول232 kb] لدى 25% من هؤلاء (8)؛ حيث قد يؤدّي أيٌّ من هذين الحذفين إلى زوال بعض العناصر المنظّمة للتعبير الجيني عند الأليل السليم من جين GJB2 (9،10). إن هذا الترافق الملحوظ لطفرات جين GJB6 مع طفرات جين GJB2 قد سوَّغ لمعظم الدراسات العالمية أن تقتصر على تقصي طفرات جين GJB6 لدى الصمّ متغايري الزيجوت heterozygous بالنسبة لإحدى طفرات جين GJB2.
وعلى الرغم من انتشار حالات فقد السمع الخلقي في المجتمع السوري، مازالت الدراسات المعنية بهذه الإعاقة الحسية في بداياتها ولا توجد حتى الآن معلومات واضحة عن تواتر الطفرات المسبِّبة، باستثناء طفرات الإكسون الثاني من جين GJB2 (12،11). وبالتالي فإن العديد من حالات الصمم لدينا مازالت مجهولة العامل الوراثي المسبِّب. وهنا نقدّم أول دراسة في سورية تستهدف كلاً من طفرتي جين GJB6 [del(GJB6-D13S1830) وdel(GJB6-D13S1845)] لدى مجموعة من مرضى فقد السمع الخلقي المتنحي غير المرافق للمتلازمات الذين دُرست لديهم سابقاً طفرات الإكسون الثاني من جين GJB2 (12). هدفت دراستنا إلى معرفة تواتر طفرتي جين GJB6 وتواتر ترافقهما مع طفرات جين GJB2 للتأكد من مدى فعالية التشخيص الجزيئي وكفاية المشورة الوراثية إن اقتصرا في تقصي طفرات جين GJB6 على الصمّ متغايري الزيجوت بالنسبة لإحدى طفرات جين GJB2 توفيراً للوقت والكلفة.
|
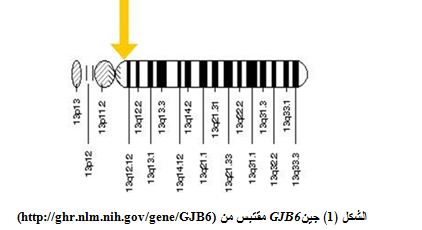 |
| المواد والطرقMaterials and Methods |
جرى انتقاء أفراد الدراسة من 41 عائلة سورية مختلفة، حيث انتقي فرد واحد مصاب بفقد للسمع من كل عائلة، على أن تكون القصة العائلية ترجّح إصابتهم بفقد السمع لأسباب وراثية، وبصفة متنحية، وبشكل غير مرتبط بمتلازمات فقد السمع.
جرى تحري الطفرتين del(GJB6-D13S1830) وdel(GJB6-D13S1854) في تفاعلين منفصلين باستخدام مشارع مقتبسة من الأدبيات الطبية (5، 8)، ومصنّعة من قبل شركة VBC-Biotech النمساوية بتركيز نهائي 0.5 µM، وعتيدة HotStar PCR SuperMix kit صنع شركة GeneDirex الأمريكية على جهاز MasterCycler pro S صنع شركة Eppendorf الألمانية.
تضمّن البرنامج الحراري مرحلة تفعيل إنزيم Taq DNA polymerase بدرجة 94 ْC مدة دقيقتين، وخمساً وأربعين دورة من التمسخ بدرجة 94 ْC مدة 30 ثانية، والتلدين بدرجة 58 ْC مدة 30 ثانية، والإطالة بدرجة 72 ْC مدة دقيقتين، وخُتم التفاعل بمرحلة إطالة بدرجة 72 ْC مدة سبع دقائق.
جرى تحميل نواتج التفاعلين على هلامة الأغاروز 2.5%، ثم رُحِّلت بواسطة جهاز الرحلان الكهربائي الأفقي. تم تأكيد العينات الإيجابية لأيٍّ من الطفرتين بإجراء تفاعل تحديد التسلسل النُوكْلِيُوتيدي للمنطقة المضخَّمة باستخدام العتيدة BigDye® Terminator v3.1 Cycle Sequencing kit صنع شركة Applied Biosystems الأمريكية.
وفي ما يلي المشارع المستخدمة في تحري الطفرتين (5، 8):
|
 |
| النتائجResults |
تبيّن في دراسة سابقة لطفرات الإكسون الثاني من جين GJB2 على عينة دراستنا وجود 4 من 41 متماثلي الزيجوت homozygous، و1 من 41 زيجوت متغاير مركب compound heterozygous، و2 من 41 متغايرَي الزيجوت heterozygous، و34 من 41 نمط شائع wildtype (12). في دراستنا هذه لم تُكشَف طفرة del(GJB6-D13S1830) في أيٍّ من أولئك المرضى متماثلي الزيجوت ومتغايريه بالنسبة لطفرات GJB2، بينما كُشفت بشكل متماثل الزيجوت لدى حالة واحدة من ذوي نمط جين GJB2 الشائع (2.9%). وهكذا فإننا لم نلاحظ أيّ ترافق بين طفرات الجينين GJB2 وGJB6. أمّا طفرة del(GJB6-D13S1854) فلم تُكشف في أيٍّ من أفراد العينة المدروسة. ويوضح الشكلان 2 و3 نتائج الرحلان على هلامة الأغاروز لنواتج تفاعل PCR في تفاعل تحري طفرة del(GJB6-D13S1830) وdel(GJB6-D13S1854).
1- نمط متماثل الزيجوت بالنسبة لطفرة del(GJB6-D13S1830) لطفل مصاب حيث تظهر عنده حزمة واحدة فقط بطول 460 bp الممثلة للنمط الطافر.
2- شاهد إيجابي لنمط متغاير الزيجوت بالنسبة لطفرة del(GJB6-D13S1830) حيث تظهر عنده حزمتان: الأولى بطول 460 bp والممثلة للنمط الطافر والثانية بطول 685 pb والممثلة للنمط الشائع.
3- نمط شائع بالنسبة لطفرة del(GJB6-D13S1830) لطفل مصاب، حيث تظهر عنده حزمة واحدة فقط بطول 685 bp الممثلة للنمط الشائع.
4- PCR marker (100-3000 bp)
1- PCR marker (100-3000 bp).
2- شاهد إيجابي لنمط متغاير الزيجوت بالنسبة لطفرة del(GJB6-D13S1854)، حيث تظهر عنده حزمتين: الأولى بطول 564 bp والممثلة للنمط الطافر والثانية بطول 333 bp والممثلة للنمط الشائع.
3- نمط شائع بالنسبة لطفرة del(GJB6-D13S1854) لطفل مصاب، حيث تظهر عنده حزمة واحدة فقط بطول 333 bp الممثلة للنمط الشائع.
|
| المناقشةDiscussion |
انقسمت عينة دراستنا من حيث طفرات جين GJB2 إلى أربعة مرضى متماثلي الزيجوت، وواحد ذي زيجوت متغاير مركب، واثنين متغايري الزيجوت، و34 من ذوي النمط الشائع. وإذ لم نكشف النمط متغاير الزيجوت لطفرة del(GJB6-D13S1830) في أيٍّ من حالات النمط الشائع لجين GJB2، فإن ذلك يتوافق مع الدراسات العالمية التي أكّدت عدم كشف هذه الطفرة بنمطها متغاير الزيجوت إلا مزدوجاً double heterozygous مع طفرة من طفرات جين GJB2 بنسبة قد تصل إلى 50% (7،8). لكنّنا لم نشاهد هذا الترافق في دراستنا رغم احتواء عينة الدراسة على أنماط متغايرة الزيجوت لطفرات GJB2. يمكن أن يُعزى ذلك إلى قلّة عدد تلك الحالات (حالتان فقط) في مجموعة الدراسة، ولكن قد يكون هذا العدد كافياً لكشف ترافق طفرات الجينين في بلاد تنتشر فيها طفرة del(GJB6-D13S1830)، كما في البرازيل 33.3% (13)، واليهود الأشكناز 71.4% (6)، وفنزويلا 11.1% (14)، وبريطانيا 31.5% (6)، والأرجنتين 15% (15)، وفرنسا 38.3%، وإسبانيا 24.6% (6). وهذا يشير إلى ندرة طفرة del(GJB6-D13S1830) في مجتمعاتنا وانحصارها بالمجتعات الغربية، خاصة أنها لم تكشف في أيّ من البلدان المجاورة كتركيا (16)، والأردن (1)، ومصر (3)، وقبرص (18)، وقطر (19)، وإيران (20).
من جهة أخرى فإن ورود هذه الطفرة بشكل متماثل الزيجوت ضمن مجموعة النمط الشائع لجين GJB2 بنسبة عالية 2.9%، مقارنة بالمجتمعات التي تنتشر فيها هذه الطفرة مثل الأرجنتين 2.17% (15)، واليهود الأشكناز 0.68%، وإسبانيا 0.23% وأمريكا 0.2% (6) رغم ندرة انتشارها في منطقتنا، يشير إلى دور زواج الأقارب في تكريس الطفرة في مجتمعاتنا المغلقة مما يزيد معدل ظهورها بشكل متماثل الزيجوت آخذين بعين الإعتبار أن عدد أفراد العينة الذين توجد صلة قربى بين والديهم قد بلغ 30 مريضاً (71.8%).
لتأكيد ذلك نحن بحاجة إلى مزيد من الدراسات التي تستهدف هذه الطفرة في عينة أكبر من المرضى المصابين بالإضافة للحملة اللاعرضيين في المجتمع السوري.
أما بالنسبة للطفرة del(GJB6-D13S1854) فإنّها لم تُكشف في أيٍّ من أفراد دراستنا كما هو الحال في البلدان المجاورة كتركيا (16)، والأردن (17)، ومصر (3)، وقبرص (18)، وقطر (19)، وإيران (20) وبعض الدول الأجنبية كفرنسا، وبلجيكا، وأستراليا، والولايات المتحدة الأمريكية (8) وفنزويلا (14). وهذا قد يعزز من احتمالية إنحصارهذه الطفرة بمجتمعات معينة كإسبانيا، والمملكة المتحدة، وإيطاليا (8) والأرجنتين (15).
ولتأكيد ما سبق أيضاً نحن بحاجة لمزيد من الدراسات التي تستهدف هذه الطفرة في عينة أكبر من المرضى السوريين المصابين بفقد السمع الخلقي بالإضافة إلى تحري هذه الطفرة عند الحملة اللاعرضيين.
|
| الاستنتاج Conclusion |
| تشير نتائج دراستنا إلى ندرة طفرة del(GJB6-D13S1830) في المرضى السوريين ذوي فقد السمع الخلقي المتنحّي غير المرافق للمتلازمات، لكنّها لا تنفي وجودها لديهم. لذا فإنّ الاقتصار في تحري هذه الطفرة على المرضى متغايري الزيجوت لطفرات GJB2 لا يضمن كفاءة التشخيص الجزيئي وكفاية المشورة الوراثية لدى أولئك المرضى؛ وإنما يُنصح بتحرّيها لدى أي مريض يعاني من فقد السمع الخلقي بخلاف طفرة del(GJB6-D13S1854) التي لا يرجَّح الاشتباه بها في مجتمعنا. |
| المراجع References |
1- Gardner P; Oitmaa E; Messner A; Hoefsloot L; Metspalu A. and Schrijver I.
Simultaneous multigene mutation detection in patients with sensorineural hearing loss through a novel diagnostic microarray: a new approach for newborn screening follow-up.
Pediatrics, 118 (3): 985-994, 2006.
2- Cordeiro-Silva Mde F; Barbosa A; Santiago M; Provetti M. and Rabbi-Bortolini E.
Prevalence of 35delG/GJB2 and del (GJB6-D13S1830) mutations in patients with non-syndromic deafness from a population of Espírito Santo-Brazil.
Braz J Otorhinolaryngol, 76(4): 428-432, 2010.
3- Elbagourya N.M; Solimana H.N; Mohammed O.S; Ghorab E.A; Elruby M.O; El-bassyounib H.T and Essawia M.L.
Mutation analysis of the GJB2 and GJB6 genes in Egyptian patients with autosomal recessive sensorineural nonsyndromic hearing loss.
Middle East J Med Genet, 3: 11-15, 2014.
4- del Castillo I; Villamar M; Moreno-Pelayo M.A; del Castillo F.J; Alvarez A; Tellería D; Menéndez I. and Moreno F.
A deletion involving the connexin 30 gene in nonsyndromic hearing impairment.
N Engl J Med, 346 (4): 243-249, 2002.
5- Batissoco A.C; Auricchio M.T.B.M; Kimura L; Tabith-Junior A. and Mingroni-Netto R.C.
A novel missense mutation p.L76P in the GJB2 gene causing nonsyndromic recessive deafness in a Brazilian family.
Brazilian Journal of Medical and Biological Research, 42: 168-171, 2009.
6- Del Castillo I; Moreno-Pelayo M.A; Del Castillo F.J; Brownstein Z; Marlin S; Adina Q; Cockburn D.J; Pandya A; Siemering K.R; Chamberlin G.P; Ballana E; Wuyts W; Maciel-Guerra AT; Alvarez A; Villamar M; Shohat M; Abeliovich D; Dahl HH; Estivill X; Gasparini P; Hutchin T; Nance WE; Sartorato EL; Smith RJ; Van Camp G; Avraham KB; Petit C. and Moreno F.
Prevalence and evolutionary origins of the del(GJB6-D13S1830) mutation in the DFNB1 locus in hearing-impaired subjects: a multicenter study.
Am J Hum Genet, 73 (6): 1452-1458, 2003.
7- Seeman P; Bendová O; Rasková D; Malíková M; Groh D. and Kabelka Z.
Double heterozygosity with mutations involving both the GJB2 and GJB6 genes is a possible, but very rare, cause of congenital deafness in the Czech population.
Ann Hum Genet; 69 (Pt 1): 9-14; 2005.
8- del Castillo F.J; Rodríguez-Ballesteros M; Alvarez A; Hutchin T; Leonardi E; de Oliveira C.A; Azaiez H; Brownstein Z; Avenarius M.R; Marlin S; Pandya A; Shahin H; Siemering K.R; Weil D; Wuyts W; Aguirre L.A; Martín Y; Moreno-Pelayo M.A; Villamar M; Avraham K.B; Dahl H.H; Kanaan M; Nance W.E; Petit C; Smith R.J; Van Camp G; Sartorato E.L; Murgia A; Moreno F. and del Castillo I.
A novel deletion involving the connexin-30 gene, del(GJB6-d13s1854), found in trans with mutations in the GJB2 gene (connexin-26) in subjects with DFNB1 non-syndromic hearing impairment.
J Med Genet; 42 (7): 588-594; 2005.
9- Rodriguez-Paris J; Tamayo M.L; Gelvez N. and Schrijver I.
Allele-specific impairment of GJB2 expression by GJB6 deletion del(GJB6-D13S1854).
PLoS One 6:e21665, 2011.
10- Rodriguez-Paris J. and Schrijver I.
The digenic hypothesis unraveled: the GJB6 del(GJB6-D13S1830) mutation causes allele-specific loss of GJB2 expression in cis.
Biochem Biophys Res Commun, 389: 354-359, 2009.
11- Al-Achkar W; Moassass F; Al-Halabi B. and Al-Ablog A.
Mutations of the Connexin 26 gene in families with non-syndromic hearing loss.
Mol Med Rep, 4: 331-335, 2011.
12- Mahayri Z.N. and Monem F.S.
GJB2 gene mutations in Syrians with sensorineural hearing loss.
Middle East Journal of Medical Genetics, 1: 80-84, 2012.
13- Belintani P.V; Maria G.B.E; Lúcia S.E. and Victor M.J.
Prevalence of the GJB2 mutations and the del(GJB6-D13S1830) mutation in Brazilian patients with deafness.
Hear Res, 196 (1-2): 87-93, 2004.
14- Utrera R; Ridaura V; Rodríguez Y; Rojas MJ; Mago L; Angeli S. and Henríquez O.
Detection of the 35delG/GJB2 and del(GJB6-D13S1830) mutations in Venezuelan patients with autosomal recessive nonsyndromic hearing loss.
Genet Test, 11(4): 347-452, 2007.
15- Gravina L.P; Foncuberta M.E; Prieto M.E; Garrido J; Barreiro C. and Chertkoff L.
Prevalence of DFNB1 mutations in Argentinean children with non-syndromic deafness.Report of a novel mutation in GJB2.
Int J Pediatr Otorhinolaryngol, 74 (3): 250-254, 2010.
16- Tarkan Ö; Sari P; Demirhan O; Kiroğlu M; Tuncer Ü; Sürmelioğlu Ö; Ozdemir S; Yilmaz M.B. and Kara K.
Connexin 26 and 30 mutations in paediatric patients with congenital, non-syndromic hearing loss treated with cochlear implantation in Mediterranean Turkey.
J Laryngol Otol, 127 (1): 33-37, 2013.
17- Mahasneh A.A. and Al-Asseer M.H.
Screening of GJB6 gene for the 342-kb deletion in patients from Jordan with non syndromic hearing loss.
Int J Hum Genet, 5: 253-257, 2005.
18- Neocleous V; Costi C; Shammas C; Spanou E; Anastasiadou V; Tanteles G.A. and Phylactou L.A.
Spectrum of GJB2 mutations in Cypriot nonsyndromic hearing loss subjects.
J Genet, 93 (2): 471-476, 2014.
19- Al Kowari M.K; Gasparini P; Abdulhadi K; Siam R; Najjar N; Al-Sulaiteen M; Dipresa S; Badii R. and Girotto G.
Mutations in GJB2, GJB6 and mDNA 1555A>G variant explain only a minority of cases of nonsyndromic hearing loss in the Qatari population.
Qatar Foundation Annual Research Forum Proceedings 2010, BMO4.
20- Tabatabaiefar M.A; Montazer Z.M; Shariati L; Saffari C.J; Ashrafi K; Gholami A; Farrokhi E; Hashemzadeh C.M. and. Noori-Daloii M.R.
Mutation Analysis of GJB2 and GJB6 Genes and the Genetic Linkage Analysis of Five Common DFNB Loci in the Iranian Families with Autosomal Recessive Non-Syndromic Hearing Loss.
Journal of Sciences, Islamic Republic of Iran, 21:105-112, 2010.
|
| |
| |
| المجلد 7 ,
العددان 9-10
, ربيع الثاني 1437 - كانون الثاني (يناير) 2016 |
|
|
|
