| المجلد 8 ,
العدد 5
, ربيع الآخر 1439 - كانون الثاني (يناير) 2018 |
| |
| تقصي جين V-ATPase subunit C لدى سلالة سورية لليشمانية المدارية |
| Investigation of V-ATPase Subunit C Gene in Syrian Strain
of Leishmania Tropica
|
| د. أميرة عرابي1، أ. د. محمد معروف1، 2، أ. د. مصطفى العموري1 |
| Orabi A.1 Maarouf M.1,2 and AL amouri M 1 |
1 كلية الصيدلة ،2 مركز الدراسات الوبائية والبيولوجية لطفيليات الليشمانية، جامعة دمشق
1Faculty of pharmacy, 2LECBS, Damascus University
|
| الملخص Abstract |
يعد داء الليشمانيات الجلدية Cutaneous Leishmaniasisداءً مستوطناً في سورية، وازداد انتشاره بشكل كبير منذ العام 2011 في سورية، وتعود معظم العداوى إلى الليشمانية المدارية L.tropica. تركز الدراسات الحالية على إيجاد لقاح فعال يقي من العدوى بداء الليشمانيات. وتعد لقاحات الدنا طريقة واعدة للحماية من العدوى.
يلعب إنزيم V-ATPase دوراً هاماً في دورة حياة الطفيلي، حيث أن وظيفته تحميض الحيز الداخلي في الخلايا حقيقية النوى. في هذه الدراسة اخترنا تحت الوحيدة V-ATPase subunit C، التي هي جزء من هذا الإنزيم، لتصميم لقاح دنا DNA ضد عداوى الليشمانية المدارية.
هدفت دراستنا إلى استقصاء جين ATPase subunit C لدى سلالة سورية لمشيقات الليشمانية المدارية (LCED Syrian 01) والتعبير عنها. جرى عزل الدنا DNA والرنا RNA من هذه الطفيليات، واصطنع الدنا المتمم cDNA، وصُممت المشارع الضرورية لتضخيم الجين بالشروط المثالية للـ PCR، جرى إثبات وجود هذا الجين لدى مشيقات الليشمانية المدارية وكان حجمه الجين 675 زوج أساس تقريباً. أُثبت أيضاً وجود تعبير عن هذا الجين لدى هذه الطفيليات، من خلال إثبات وجوده في الرنا المستخلص من مشيقات الليشمانية المدارية وتضخيم الدنا المتمم لهذا الجين.
|
Cutaneous Leishmaniasis is considered endemic disease in Syria. The spread of Leishmaniasis has significantly increased since 2011 in Syria, and most infections are caused by Leishmania tropica. Current studies focus on finding out efficient vaccine that prevents the infection with leishmania. DNA vaccines are considered a promising approach to protect from this infection. V-ATPase enzyme has essential role in the life cycle of parasite, where its function to acidify intracellular compartments in eukaryotic cells. In this study we have chosen V-ATPase subunit C, which is a part of this enzyme, to design DNA vaccine against leishmania tropica infections.
Our study aimed to investigate ATPase subunit C gene in Syrian strain of L.tropica (LCED syrian 01) promastigotes and their expression. DNA and RNA were isolated from these parasites, synthesized cDNA, designed the necessary primers for gene amplification and optimization of PCR conditions. The existence of this gene in L.tropica promastigotes has been proved and its size was approximately 675 bp. Expression of this gene was also proved in these parasites, through proving its existence in extracted RNA of Leishmania tropica promastigotes and amplfication the complementary DNA of this gene.
|
| المقدمة Introduction |
يشكل داء الليشمانيات معقداً من الأمراض تسببها طفيليات من الحيوانات الأوالي Protozoa، تنتمي إلى جنس الليشمانية Leishmania الذي يضم أكثر من 20 نوعاً من طفيلي الليشمانية. وتنتقل الإصابة إلى الإنسان عن طريق لدغة أنثى ذبابة الرمل (Johannes Gutenberg, 2007) (1). ويصنف داء الليشمانيات إلى ثلاثة أشكال: حشوي وجلدي وجلدي مخاطي. يشكل انتشار الليشمانية مشكلة صحية وخيمة متفاقمة، حيث يرتفع معدل الإصابة إلى 2 مليون سنوياً على مستوى العالم. ويعيش حوالي 350 مليون شخص حول العالم في اختطار الإصابة كل يوم، نظراً لتمركزهم في المناطق التي يستوطن فيها الطفيلي (WHO, 2014) (2). تشخص أكثر من 90% من الإصابات الجلدية في العالم في 10 دول، واحدة منها سورية. وتعود معظم الإصابات إلى الليشمانية المدارية بشكل رئيسي، وعادة ما يتميز هذا الداء بانتشار كبير في الأماكن المكتظة بالسكان، ولاسيما في مناطق الحرب والصراعات، وفي الأماكن التي توجد فيها هجرات واسعة النطاق للسكان ، مما أدى إلى ارتفاع الإصابات بشكل كبير في سورية في ظل الحرب (Hayani et al. 2015) (3)، ووفقاً لتقارير صادرة عن منظمة الصحة العالمية، سجل عدد الإصابات بالليشمانية عام 2013 ضعفي متوسط الإصابات بين عامي 2004 و2008، الذي كان يسجل 100 ألف إصابة سنوياً (WHO, 2017) (4). تترواح الإصابات بين آفات جلدية سليمة العواقب إلى أذيات جهازية متنوعة قد تكون قاتلة. تركز الدراسات الحالية على إيجاد لقاح فعال يقي من العداوى بداء الليشمانيات، وتشكل لقاحات الدنا مقاربة واعدة في مجال الحماية من هذه العداوى. يتطلب تصميم لقاح جيني فعال يقي من عداوى الليشمانية المدارية توافر معلومات مفصلة عن جينوم الطفيلي، ونظراً لأن الدراسات التي نشرت حول جينوم الليشمانية المدارية محدودة جداً، فقد قررنا التوسع في دراستها، وخاصة دراسة الجينات التي تلعب دوراً هاماً في حياة الطفيلي، وذلك بهدف تصميم لقاح دنا مستقبلي يقي من الإصابة بهذه الطفيليات.
توجهت دراستنا إلى تحت الوحيدة V-ATPase subunit C التي تشكل جزءاً من إنزيم الأدينوزين ثلاثي الفسفاتاز الفجوي V-ATPase وذلك نظراً لدوره الهام جداً لدى حقيقيات النوى جميعها، حيث يعمل على رفع درجة حموضة الحيز داخل الخلوي لدى حقيقيات النوى وتحقيق التوازن الأيوني معتمداً بذلك على حلمهة الـ ATP (Vladimir M. 2014) (5). وهو عبارة عن معقد كبير يتألف من قسمين وظيفيين هما V1 وV0، يحتوي القسم V1 على ثماني وحيدات (A-H) ويكون مسؤولاً عن حلمهة الأدينوزين ثلاثي الفسفات ATP، ويحتوي القسم V0 على خمس وحيدات ويكون مسؤولاً عن نقل البروتونات. وفي الحقيقة تلعب الوحيدة C دوراً جوهرياً في ضبط عملية تجميع وانفصال كل من قطاعي الإنزيم، وتعد هذه الآلية هامة جداً في ضبط فعالية عمل الإنزيم في الخلايا (Stevens T.H. 1997) (6). في البداية كان لابد من إثبات وجود جينV-ATPase subunit C لدى الليشمانية المدارية المنتشرة في سورية، وتحري التعبير عن الجين على مستوى الدنا المتمم لطفيليات الليشمانية المدارية.
|
| المواد والطرقMaterials and Methods |
- تصميم مشارع لتضخيم جين V-ATPase subunit C
جرت دراسة تسلسلات الجينات لدى الأنواع الأخرى من الليشمانية (الكبيرة والطفلية والدونوفانية والمكسيكية ) باستخدام برنامجي Vector NTI Express وCLC free workbench والتطبيقات التالية:
http://www.ebi.ac.uk/Tools/services/web/toolresult.ebi?jobId=clustalw2-I20140817-223745-0957-17979833-oy
http://www.ebi.ac.uk/Tools/psa/emboss-needle/nucleotide.html
صممت المشارع باستخدام التطبيقات التالية:
http://eu.idtdna.com/calc/analyzer
http://www.geneinfinity.org/sms/sms-primanalysis.html
أضيفـت تسلسلات التعرف لإنزيمي ECORI وEXBI لـتسلسل المشارع المستخدمـة لتضخـيم جيـن V-ATPase subunit C. اختيرت الإنزيمات السابقة لأنها تسمح بإتمام العمل في خطوة لاحقة وتنسيل هذه الجينات في بلازميد PCI
لتصميم لقاح دنا يحوي الجين، وتقييم قدرته الاستمناعية لدى فئران التجربة BALB/c. صُنعت مشارع عالية النقاوة وفقاً للتسلسلات التي قمنا باختيارها من قبل شركة Alpha DNA الكندية.
التسلسل النهائي للمشارع اللازمة لتضخيم جين V-ATPase subunit C:
المشرع المباشر:
5`- GGAATTC AT GCC TGT GGA AGC GGA AGT-3`
المشرع العكسي:
5`- GCTCTAGACTACTTCATTTGA
ACCTTCTGCG-3`
تسلسل التعرف لإنزيم ECORI: GAATTC تسلسل التعرف لإنزيم XBAI: TCTAGAs
- تضخيم الجينV-ATPase subunit C باستخدام المشارع النوعية له على مستوى الدنا والدنا المتمم
1- جرى استخلاص الدنا من مشيقات Promastigote طفيليات الليشمانية المدارية وذلك بعد زرع مشيقات من سلالة LCED Syrian 01 من طفيليات الليشمانية المدارية L. tropica المأخوذة من مركز الدراسات الوبائية والبيولوجية لطفيليات الليشمانية وجرى عزل الدنا من الطفيليات المزروعة على وسط PRMI-1640 لشركة Lonzaالأميركية والمدعم بمصل العجل الجنيني منزوع المتممة لشركة Cytogen الأميركية، باستخدام عتيدة عزل الدنا من شـركة
Thermo Scientific الأمريكية.
2- جرى استخلاص الرنا RNA من طفيليات الليشمانية باستخدام عتيدة عزل الرنا GeneJET RNA purification من شركة Thermo Scientific الأميركية.
3- جرى اصطناع الدنا المتمم cDNA من الرنا المستخلص من طفيليات الليشمانية المدارية باستخدام عتيدة اصطناع الدنا المتمم Revert Aid First Strand cDNA Synthesis من شركة Thermo Scientific الأمريكية.
4- جرى تضخيم الدنا DNA والدنا المتمم cDNA لجينV-ATPase subunit C بتفاعل البوليميراز التسلسلي PCR.
استخدمت عتيدة PCR Master Mix من شركةThermo Scientific الأمريكية، صنعت المشارع التي قمنا بتصميمها بنقاوة عالية من قبل شركة Alpha DNA الكندية. جرى تضخيم الجين V-ATPase subunit C باستخدام المشارع الخاصة التي صممناها.
جرت أمثلة شروط تفاعل البوليميراز التسلسلي المطلوب لتضخيم الجين باستخدام برنامج التدرج الحراري gradient لاختيار درجة حرارة الالتحام الملائمة.
يتألف مزيج تفاعل الجين من المكونات التالية: 1 مكل من محلول المشرع المباشر ذي التركيز 10 مكرومول، 1 مكل من محلول المشرع العكسي ذي التركيز 10 مكرومول، 2.5 مكل من المرصاف سواء دنا أو دنا متمم، 12.5 مكل من PCR Master Mix، 8 مكل ماء PCR. وكان تفاعلPCR لجين V-ATPase subunit C كما يلي: دورة واحدة من التمسخ البدئي لمدة 5 دقائق بدرجة حرارة 95° C و35 دورة تتألف كل منها من: التمسخ لمدة 1 دقيقة بدرجة حرارة 95° Cوالالتحام لمدة 45 ثانية بدرجة حرارة 58.5°C والاستطالة لمدة 1 دقيقة بدرجة حرارة 72° C.
الرحلان الكهربائي لنواتج تضخيم الجين
فُصلت نواتج PCR للجين المضخم على هلامة أغاروز تركيزها 1% ملونة ببروميد الإيثيديوم.
|
| النتائج Results |
- تقييم جودة الدنا المستخلص من طفيليات الليشمانية المدارية
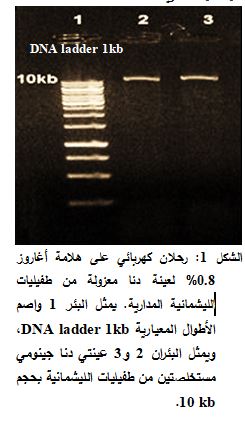
أظهر ترحيل الدنا المستخلص من الطفيليات على هلامة أغاروز بتركيز 0.8% وجود عصابة واحدة، مما يشير إلى جودة استخلاص الدنا وعدم تدركه. جرت معايرة الدنا المستخلص من 100 مليون من طفيليات الليشمانية المدارية، وقيست نقاوته فكان تركيز الدنا المستخلص مساويا 175 نانوغرام/مكل، وكانت النسبة A260\A280 تساوي 1.65، مما يشير إلى نقاوة عالية لعينة الدنا المستخلصة وخلوها بشكل شبه كامل من البروتينات (الشكل 1).
- أمثلة شروط تفاعل البوليميراز التسلسلي PCR للجين V-ATPase subunit C
جرت أمثلة شروط تفاعل تضخيم الجين وجرى التضخيم وفقاً للبروتكول المذكور سابقاً في فقرة الطرق. وتمكنا من تحديد درجة الالتحام المثلى للمشارع المصممة للجين، بعد إجراء تفاعل حراري متدرج وكانت 58.5°C.
- نتائج تضخيم الجين V-ATPase subunit C
أظهرت نتائج الرحلان الكهربائي على هلامة أغاروز 1% لناتج تفاعل التضخيم التسلسلي لجين V-ATPase subunit C، باستخدام المشرع المباشر والمشرع العكسي، وجود عصابة واحدة فقط (الشكل 2)، بطول bp 675 تقريباً. يعكس وجود عصابة واحدة تضخيم الجين المطلوب فقط، مما يظهر نوعية المشارع المصممة لهذا الجين. وهكذا نكون قد أثبتنا وجود جين V-ATPase subunit C ضمن جينوم الليشمانية المدارية المستخدمة في دراستنا بطول جين مماثل لطول الجين لدى الليشمانية الطفلية والكبيرة والمكسيكية والدنوفانية.
- تقييم جودة الرنا RNA المستخلص من طفيليات الليشمانية المدارية
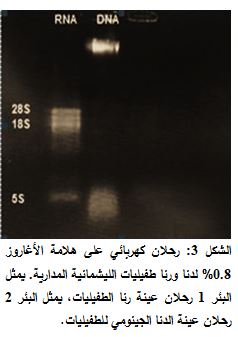
جرى التأكد من جودة الرنا المستخلص من الطفيليات، حيث قيست نقاوته بوساطة جهازNANO DROP وبلغت 2,3 وبلغ تركيز العينة 1600 نانوغرام/مكل وبلغ مردود الاستخلاص 56 مكغ. أظهر ترحيل عينة الرنا المستخلصة بواسطة الرحلان الكهربائي الأفقي على هلامة أغاروز بتركيز 0.8%، بعد تعريض الهلامة لمنبع الأشعة فوق البنفسجية، وجود عصابتي s28 وs18 واضحتين وعصابة5S ، بينما لم يظهر عصابة للدنا، مما يدل على عدم تلوث الرنا بالدنا الجينومي (الشكل 3).
- تضخيم الدنا المتمم للجين V- ATPase subunit C
أظهرت نتائج الرحلان الكهربائي على هلامة الأغاروز 1% لناتج تفاعل البوليميراز التسلسلي لجين V-ATPase subunit C باستخدام المشرع المباشر والمشرع العكسي (الشكل 3)، وجود عصابة واحدة بطول bp 675 تقريباً، مما يدل على حدوث التعبير عن هذا الجين ضمن الليشمانية المدارية.
|

 |
| المناقشة Discussion |
يعد داء الليشمانيات الجلدية داءً مستوطناً في سورية ومنطقة الشرق الأوسط. يترك الداء الجلدي ندباً مشوهة بعد الشفاء، و يسببه في سورية نوعان من الطفيليات هما الليشمانية المدارية بشكل رئيسي والليشمانية الكبيرة. وتشير تقارير منظمة الصحة العالمية إلى ارتفاع عدد الإصابات بداء الليشمانيات الجلدية في 5 دول، منها سورية، إلى أكثر من 10000 إصابة جديدة في العام 2015 (Postigo J; 2015) (7).في ظل انعدام وجود دواء نوعي آمن وفعال وعدم توافر لقاح فعال حتى الآن، تشكل لقاحات الدنا خياراً واعداً في القضاء على داء الليشمانيات ((Sukuaran et al, 2004 (8). تمتاز هذه اللقاحات بقدرتها على تفعيل استجابة مناعية من نمط Th1، والتي تلعب دوراً هاماً في شفاء العداوى بطفيليات الليشمانية Schroeder J; 2011)) (9). نظراً لتفاقم المشكلة، يشكل البحث عن لقاح تحدياً كبيراً للباحثين، وخاصة الباحثين السوريين.
يتطلب البحث عن لقاح جيني فعال توافر معلومات مفصلة عن جينات عوامل الفوعة للطفيليات المنتشرة في سورية، وبشكل خاص الليشمانية المدارية، ومعلومات عن الدور الوظيفي لهذه الجينات. ويعود السبب الرئيسي لاختيار الجينات التي يمكن استخدامها في اللقاح الجيني إلى أهمية هذه الجينات في حياة الطفيلي وقدرتها الاستمناعية، وقدرتها على تحريض وقاية طويلة الأمد تجاه العدوى بطفيليات الليشمانية. وفي الحقيقة تشكل الوحيدة V-ATPase subunit C جزءاً من إنزيم V-ATPase، الذي يلعب دوراً أساسياً في حياة حقيقيات النوى جميعها، حيث يلعب دوراً في نقل البروتونات عبر الأغشية الخلوية في عدد كبير من الخلايا (Vladimir M; 2014) (5)، مما لفت انتباهنا إلى إمكانية استخدام هذا الجين كلقاح ودراسة قدرته الاستمناعية للوقاية من عداوى الليشمانيات. ونظراً لعدم توافر أية دراسات عن وجود هذا الجين في جينوم الليشمانية المدارية، كان لابد من إجراء خطوة أولى تهدف إلى إثبات وجود هذا الجين ضمن جينوم الليشمانية المدارية، لنتمكن من استخدامه لاحقاً في تصميم لقاح ودراسة قدرته الإستمناعية في الوقاية من الإصابة.
يتطلب إثبات وجود الجين استخدام مشارع نوعية تسمح بتضخيمه بوساطة تفاعل البوليميراز التسلسلي PCR. يتطلب تصميم المشارع مقارنة تطابق تسلسلات الجين لدى الأنواع الأخرى من الليشمانية. لذلك أجريت دراسة حاسوبية لتسلسلات هذا الجين عند أنواع أخرى من الليشمانية كالليشمانية الكبيرة، والدنوفانية، والطفلية، والمكسيكية. سمحت الدراسة الحاسوبية بمعرفة مدى التطابق بين تسلسلات الجين في هذه الأنواع ومدى التطابق بين هذه التسلسلات والجينوم البشري الذي بلغ 23% فقط، وبالتالي تمكنا من تصميم المشارع المناسبة لتضخيم الجين. ومن ثم جرت أمثلة الشروط لتفاعل البوليميراز التسلسلي، وحصلنا على تضخيم جيد للجين. مما أثبت نوعية المشارع التي قمنا بتصميمها، وسمح ترحيل نواتج تفاعل PCR لتضخيم الجين بالحكم على نوعية المشارع، نتيجة لوجود عصابة وحيدة تعبر فقط عن الجين المطلوب تضخيمه، حيث بلغ حجمه 675 زوج أساس تقريباً. تماثل حجم هذا الجين لدى الليشمانية المدارية مع حجمه لدى باقي أنواع الليشمانية حيث بلغ حجمه 675 زوج أساس لدى الليشمانية الكبيرة والطفلية والدنوفانية والمكسيكية. وبهذا نكون قد أثبتنا وجود هذا الجين في جينوم الليشمانية المدارية.
ولمعرفة قابلية التعبير عن جين V-ATPase subunit C، قمنا بعزل الرنا من طفيليات الليشمانية المدارية المستخدمة في دراستنا وقمنا بتحويله إلى الدنا المتمم cDNA، ومن ثم إجراء تفاعل PCR باستخدام الدنا المتمم كمرصاف، باستخدام المشارع النوعية للجين والتي صممناها وذكرت سابقاً. وأظهر الرحلان الكهربائي لنواتج تفاعل البوليميراز التسلسلي السابق وجود عصابة وحيدة للجين تمتلك حجم الجين نفسه والتي حصلنا عليها على مستوى الدنا، وبالتالي نكون قد أثبتنا حدوث الإنتساخ الذي يشكل المرحلة الأولى من مراحل التعبير الجيني. تسمح النتائج السابقة بإمكانية استخدام هذا الجين من الناحية التقنية والتطبيقية لتصميم لقاح ضد الليشمانية المدارية و تقييم قدرته الاستمناعية وهو أمر قيد التطبيق. كما سنجري سلسلة لهذا الجين لمقارنة التسلسل مع تسلسل الجين نفسه لدى الأنواع الأخرى من الليشمانية.
|
الاستنتاجات Conclusion
بينت هذه الدراسة وجود جينV-ATPase subunit C لدى سلالة سورية لليشمانية المدارية وبينت أيضاً التعبير عنها على مستوى الرنا لهذه الطفيليات.
|
| المراجع References |
1-Gutenberg J.
Cutaneous Leishmania infection: Progress in pathogenesis research and experimental therapy.
Experimental Dermatology, 16(6): 340-346, 2007.
2-World Health Organization.
Manual for case management of cutaneous leishmaniasis in the WHO Eastren Mediterranean Region, 2014.
3-Hayani K; Dandashli A. and Weisshaar E.
Cutaneous Leishmaniasis in Syria: Clinical Features, Current Status and the Effects of War.
Acta Dermato-Venereologica, 95(1): 62-66, 2015
4- World Health Organization.
Manual for case management of
cutaneous leishmaniasis in the WHO Eastren Mediterranean Region, 2017
5-Vladimir M; John R. and Gerhard G.
Eukaryotic V-ATPase: Novel structural findings and functional insights.
Biochimica et Biophysica Acta, 1837(6): 857-874, 2014
6-Stevens T.H. and Forgac M.
Structure, function and regulation of the vacuolar (H+) ATPase.
Annu. Rev. Cell Dev. Biol, 13(2): 779-808, 1997
7-Pstigo J.
Global leishmaniasis update, 2006-2015: a turning point in leishmaniasis surveillance.
WHO, 92(38): 557-565, 2017
8-Sukumaran B. and. Madhubala R.
Leishmaniasis: current status of vaccine development.
Current Molecular Medicine, 4(6): 667-679, 2004.
9-Schroeder J. and Aebischer T.
Vaccines for leishmaniasis: from proteome to vaccine candidates,
Human Vaccine, 7(2) :10-15, 2011.
|
| |
| |
| المجلد 8 ,
العدد 5
, ربيع الآخر 1439 - كانون الثاني (يناير) 2018 |
|
|
|
